Tras ver la teoría sobre colorantes y tinciones vamos a analizar las principales tinciones usadas en microbiología y los colorantes que las forman.
En este caso, las diferentes técnicas de tinción analizadas se usan para el microscopio óptico. La mayoría de las muestras se podrán ver en el microscopio con aumentos de 20x y 50x, aunque habrán casos donde será necesario usar el aumento 100x (donde se añade también el aceite de inmersión a la muestra).
Las tinciones principales son la de Gram y de Ziehl-Neelsen, ambas diferenciales; aunque también hay otras tinciones diferenciales y selectivas de interés para la microbiología.
Recordatorio: antes de leer este artículo sería bueno que conozcas un poco de teoría sobre las fases, mecanismos y tipos de tinciones que hay (además de las partes que tienen los colorantes). Si conoces todo esto podrás entender mejor ciertas expresiones que son más del gremio 😄.
Índice de contenidos
Tinción de Gram
La tinción de Gram es probablemente la más conocida; es de tipo diferencial y sirve para distinguir a los microorganismos por morfología y composición.
Hay que tener en cuenta que se debe hacer la tinción cuando el cultivo esta en fase exponencial, ya que en fase estacionaria (“vejez”) se pueden confundir las gram positivas con las negativas. Esto ocurre debido a la perdida de capas de peptidoglicano por parte de bacterias gram positivas.
Colorantes
- Cristal violeta. Da color azul o violáceo a las bacterias gram positivas.
- Safranina. Da color rojizo o anaranajado a las bacterias gram negativas.
Aparte de estos colorantes, en la tinción de Gram se usará el lugol como mordiente, y alcohol 96% para decolorar. Todas las células (sean Gram positivas o negativas) se teñirán con el cristal violeta.

Ahora bien, el alcohol quita fosfolípidos y cierra los poros de la pared celular, por lo que el cristal violeta queda atrapado. Las bacterias gram positivas podrán soportar este proceso gracias a su gran capa de peptidoglicano. No obstante, las bacterias Gram negativas no aguantarán este tratamiento con alcohol, por lo que se quitará el cristal violeta de ellas.
Preparación
El proceso de tinción consta de los siguientes pasos:
- Con el asa de cultivo se cogen varias cargas (colonias, células bacterianas), y se extienden por el portaobjetos. No se añade agua destilada.
- El proceso de fijación se realiza por calor a la llama.
- Se añade cristal violeta, recubriendo con este colorante el portaobjetos durante 2 o 3 minutos.
- Ahora se añade lugol (yoduro potásico 2% + yodo) durante 1 minuto. El lugol no es un colorante en sí, sino que hace de mordiente. El mordiente se acopla con el colorante y facilita su absorción por parte del microorganismo.
- Se lava el portaobjetos con agua destilada. El agua no debe tocar directamente la muestra.
- Decolorado con alcohol 96%. Se añade el alcohol gota a gota, y de la muestra saldrán gotas violáceas. Paramos de añadir alcohol cuando salga la primera gota transparente de la muestra.
- Se añade el colorante de contraste, la safranina, durante 5 minutos.
- Por último se lava el portaobjetos y se seca.
Utilidades
La principal utilidad de la tinción de Gram es la de distinguir entre bacterias gram positivas y negativas. Las gram negativas que perdieron coloración por el tratamiento con alcohol ahora se verán de color rojo, naranja o rosáceo por acción de la safranina. Por otra parte, las bacterias gram positivas teñidas con cristal violeta tendrán un color azulado o violáceo.
Gram positivas
Las siguientes especies son las gram positivas más representativas:
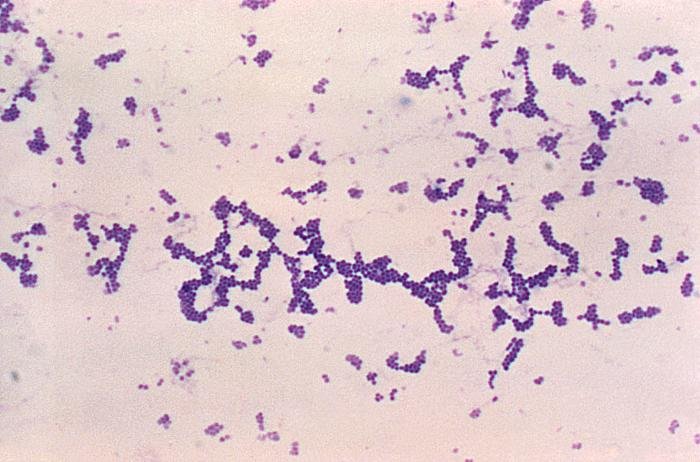
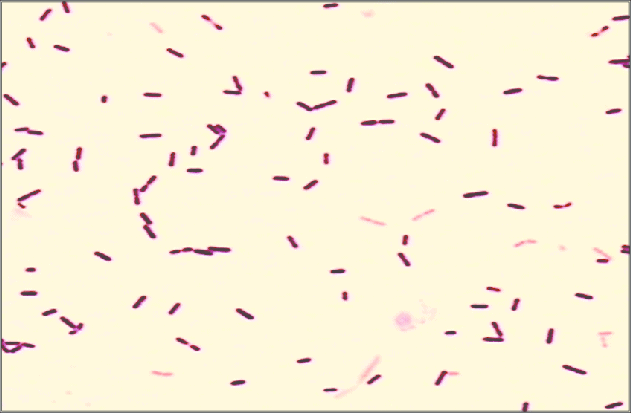
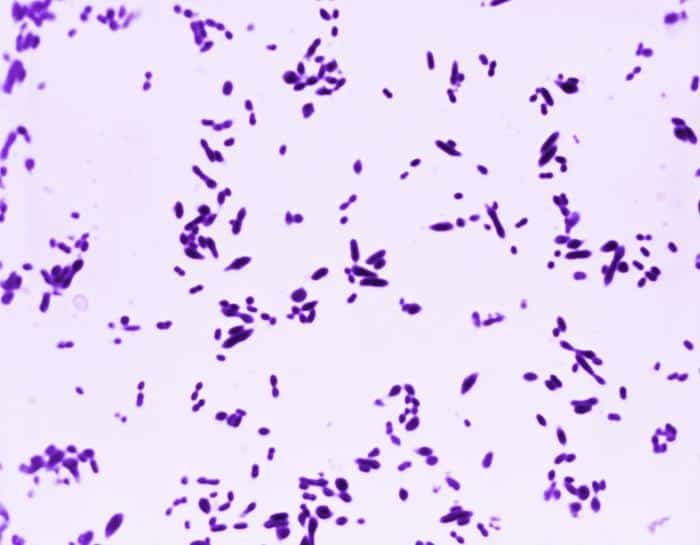
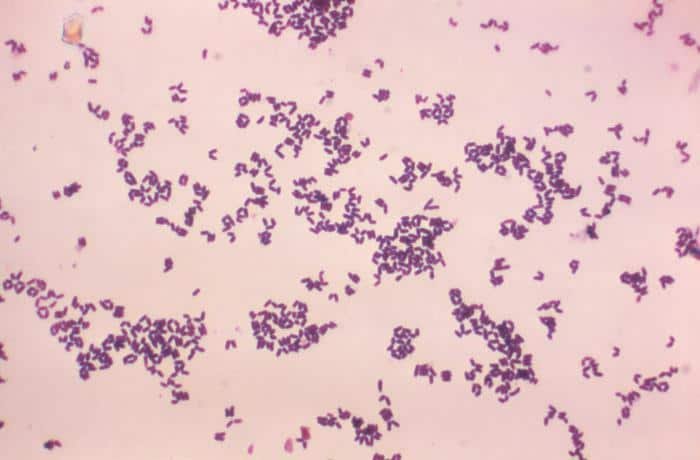

Quizá eches de menos a Mycobacterium tuberculosis. Es cierto, que es una bacteria gram positiva. No obstante, no se detecta bien con la tinción de gram. Hace falta otra tinción diferencial (tinción de Ziehl-Neelsen) que veremos más adelante.
Gram negativas
A continuación veremos algunas de las bacterias gram negativas más comunes:
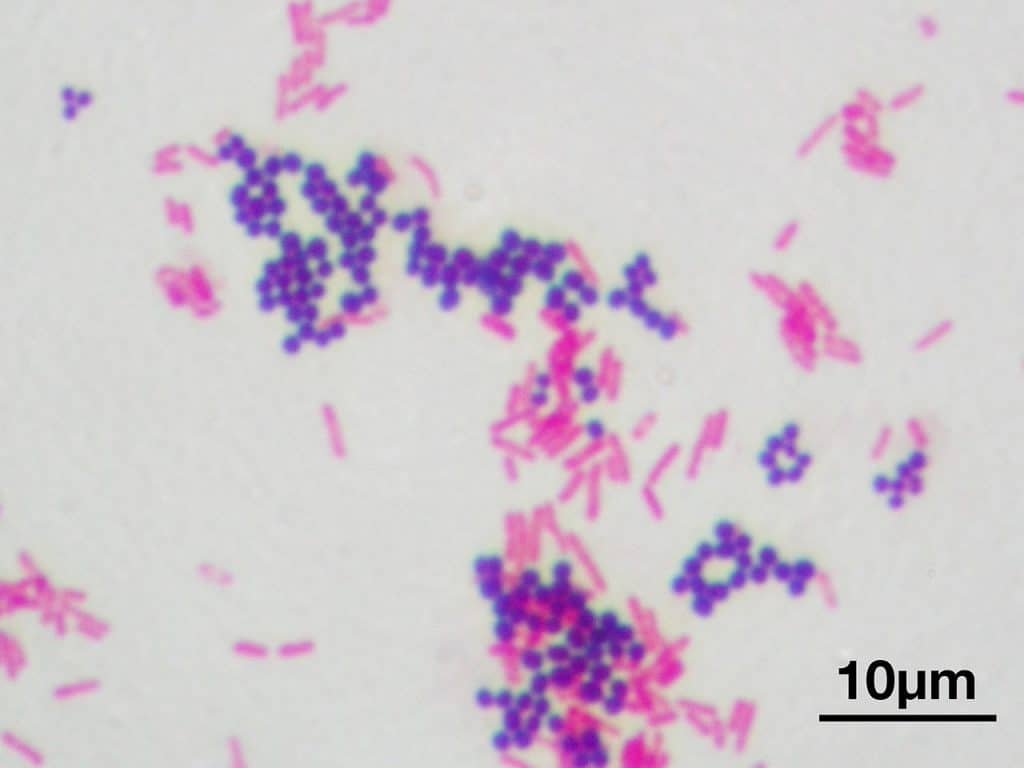
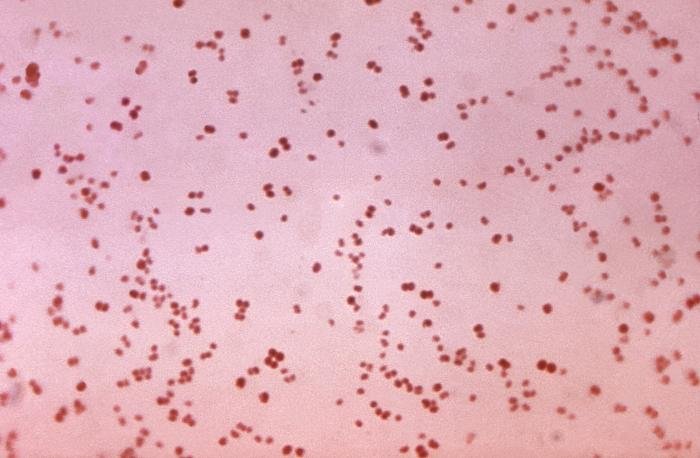
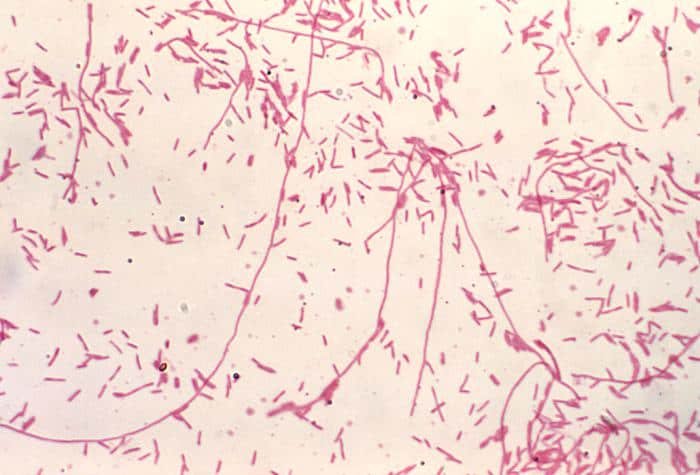

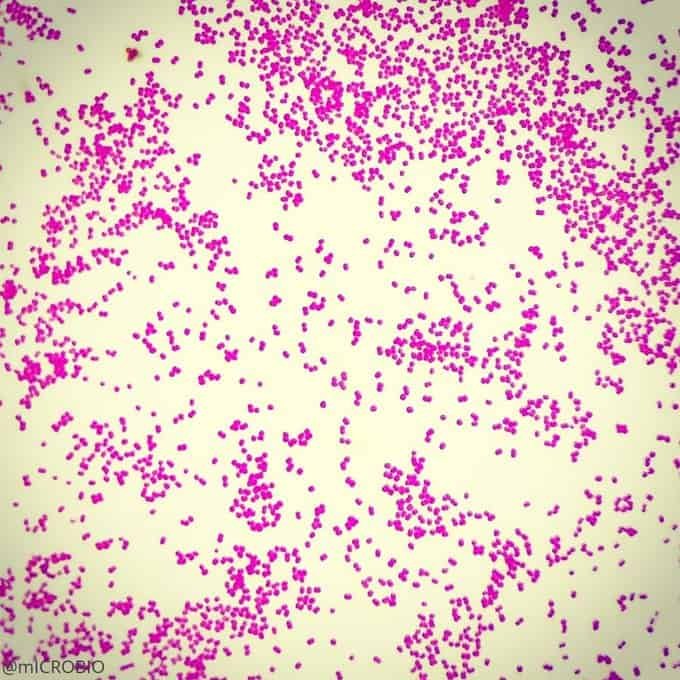
Recordatorio: las bacterias gram positivas se tiñen de azul (azul oscuro o violeta), mientras que las bacterias gram negativas se tiñen de rojo (rojo, anaranjado o rosado). A lo mejor lo tienes claro; pero en mi caso personal casi siempre las confundía. Por eso he puesto el color respectivo en cada frase, para que lo recuerdes mejor si te pasa igual que me pasaba a mí. 😉
Tinción Ziehl-Neelsen
La tinción de Ziehl-Neelsen es de tipo diferencial, y sirve para detectar bacterias ácido-alcohol resistentes (BAAR), siendo la más destacada Mycobacterium tuberculosis. Esto es muy útil, sobre todo teniendo en cuenta que M. tuberculosis no puede ser detectada correctamente con la tinción de Gram.
Lo que hace diferentes a estas bacterias es la presencia de un polímero (ácidos micólicos) que se une a azúcares, lo que provoca que el conjunto de la pared sea muy impermeable.
Colorantes
- Fucsina fenicada. Da un color rojizo a las bacterias AAR.
- Azul de metileno. Da un color azulado al resto de bacterias que no son AAR.
En la tinción de Ziehl-Neelsen, el alcohol-ácido cumple la una función parecida a la del alcohol 96% en la tinción de Gram. En este caso, el contraste aparece por los ácidos micólicos, que hacen que sus bacterias sean impermeables al alcohol-ácido. Las bacterias que no cuenten con estos ácidos micólicos se decolorarán por acción del alcohol, y la fucsina saldrá de éstos.
Preparación
El proceso de tinción consta de los siguientes pasos:
- Con el asa de cultivo se cogen varias cargas (colonias, células bacterianas), y se extienden por el portaobjetos. No se añade agua destilada.
- Se fija la muestra con calor.
- Se añade fucsina fenicada, cubriendo totalmente el portaobjetos durante 3 minutos.
- Más tarde, se pasa el mechero varias veces, durante 5 minutos, pero sin permitir que hierva el colorante, ni que se seque, ya que sino el colorante se consume.
- El exceso de colorante se quita con agua destilada.
- Se añade alcohol-ácido para la decoloración durante 10 minutos a intervalos de 1 minuto y medio.
- Ahora se añade el colorante de contraste, el azul de metileno, durante 3 minutos.
- Por último, se lava el portaobjetos y se seca al aire.
Utilidades
La principal función de la tinción de Ziehl-Neelsen es la detección de micobacterias, tales como las provocadoras de tuberculosis (M. tuberculosis) o la lepra (M. leprae). También hay otras micobacterias que, si bien no son patógenas, sí que pueden ser patógenos oportunistas en determinadas circunstancias.
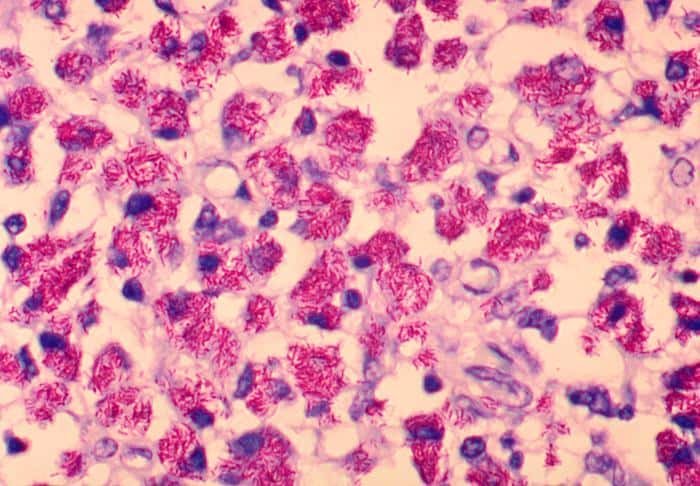
Además, se pueden detectar corinebacterias de gran interés para la biotecnología por su producción de aditivos, o a Streptomyces, formadora de diversos antibióticos. Nocardia y Actinomices también pueden aparecen como bacterias ácido-alcohol resistentes.
Las células bacterianas teñidas con fucsina aparecerán con un color rojo fuego, mientras que las teñidas con azul de metileno tendrán un color azulado.
Tinción de Wirtz-Conklin
La tinción de Wirtz-Conklin se usa para observar bien las endosporas bacterianas. La muestra debe ser obtenida de un cultivo en fase estacionaria. En este caso, para su observación al microscopio hay que usar la lente x100, usando aceite de inmersión.
Entra en el grupo de las tinciones selectivas, aunque al añadir un colorante de contraste es tecnicamente una tinción diferencial.
Colorantes
- Verde malaquita. Tiñe las endosporas de verde.
- Safranina. Es opcional, y sirve para colorear el resto de la célula con un color anaranjado.
Preparación
El proceso de tinción consta de los siguientes pasos:
- Con el asa de cultivo se cogen varias cargas (colonias, células bacterianas), y se extienden por el portaobjetos. No se añade agua destilada.
- Se fija la muestra con calor.
- Se añade verde malaquita, cubriendo totalmente el portaobjetos durante 9 minutos.
- Ahora se aplica calor de 3 a 6 minutos para que el colorante entre en las paredes de la endospora. El calor es aplicado hasta que aparezcan emisión de vapores.
- Se lava con agua el portaobjetos para retirar el colorante de la célula (a excepción de las endosporas).
- Ahora se añade el colorante de contraste, la safranina, durante 5 minutos.
- Por último, se lava con agua y se seca el portaobjetos.
Utilidades
Se usa para observan las endosporas bacterianas, estructuras de resistencia que forman algunas bacterias para sobrevivir en condicione ambientales extremas donde no pueden hacer su ciclo de vida normal. Así, se pueden ver las endosporas que forman Bacillus anthracis y Clostridium perfringens, entre otros.
Las endosporas no absorben la mayoría de los colorantes debido a sus cubiertas gruesas e impermeables. No obstante, el verde malaquita puede hacerlo, por lo que las endosporas bacterianas quedarán teñidas de verde mientras que el resto de las células bacterianas tendrán un color rosáceo.

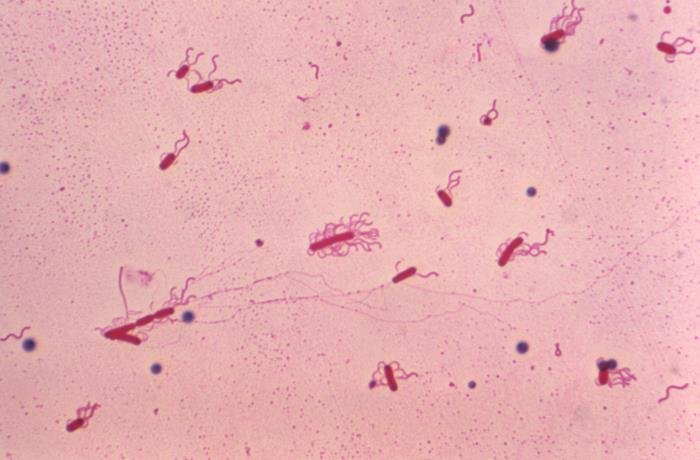
Tinción de Leifson
La tinción de Leifson usa para la observación de flagelos bacterianos; entra dentro de las tinciones selectivas. Tienen un espesor de 0.01 micrones, por lo que son invisibles al microscopio óptico; por ello hace falta esta técnica especial. Para su observación en el microscopio óptico, se debe usar aceite de inmersión y el aumento 100x.
Recalcamos el hecho de esta tinción se usa para ver flagelos bacterianos; los flagelos de organismos eucariotas son más gruesos y pueden verse con tinciones simples o incluso con preparaciones al fresco.
Colorantes
Se usa el colorante de Leifson que está formado por:
- Fucsina básica 95%. Es el colorante en sí mismo.
- Etanol 1.2%.
- Ácido tánico 3%. Tiene función de mordiente.
- Cloruro sódico 1.5%.
- Agua destilada. Aparece en unión a ácido tánico y cloruro sódico, formando parte de sus soluciones.
Las estructuras teñidas aparecen con color rojizo.
Preparación
El proceso de tinción consta de los siguientes pasos:
- Con el asa de cultivo se cogen varias cargas (colonias, células bacterianas), y se extienden por el portaobjetos. No se añade agua destilada. (Previamente se debe haber hecho un círculo en el portaobjetos).
- El proceso de fijación se realiza sin llama durante 5 minutos. No se usa el mechero ya que demasiado calor puede destruir los flagelos.
- Se añaden unas gotas del colorante de Leifson y se espera 15 minutos.
- Ahora se lava el portaobjetos con agua destilada y se seca
Utilidades
Esta tinción se usa para ver a los flagelos, algo esencial para identificar muchas especies. Y es que los flagelos pueden aparecen en número y disposición diferente en las bacterias, de ahí que sean una forma de clasificación de estas (para ver los tipos de bacterias según el número y disposición de flagelos puedes entrar en el artículo de la célula procariota, en la sección “flagelo”).
Tinción de Giemsa
Esta tinción es más usada en citología, ya que puede discriminar entre zonas con altos contenidos de ADN, por lo que puede diferenciar diversos orgánulos de la célula; es una tinción diferencial. No obstante, también se usa en microbiología para la detección de ciertas bacterias, destacando Rickettsia.
Colorantes
Colorante de Giemsa. Da un color azul oscuro o violáceo al microorganismo objetivo.
Preparación
El proceso de tinción consta de los siguientes pasos:
- Con el asa de cultivo se cogen varias cargas (colonias, células bacterianas), y se extienden por el portaobjetos.
- El proceso de fijación se realiza con metanol durante 3 o 5 minutos.
- Se añaden unas el colorante de Giemsa y se espera 8 minutos.
- Ahora se lava el portaobjetos con agua destilada y se seca
Utilidades
En microbiología, la tinción de Giemsa detecta a bacterias como Rickettsia y Chlamydia, a protistas como Plasmodium y Pneumocystis, y ciertos hongos, como Histoplasma. Dichos microorganismos se detectan en posibles células infectadas.

Otro patógeno importante que detecta la tinción de Giemsa es Helicobacter pylori, causante de gastritis y úlceras.

No obstante, esta tinción es más usada en citología.
Tinción negativa
Se usa para detectar las cápsulas que aparecen en algunas bacterias, así que entra en el grupo de las tinciones selectivas. La tinción negativa se puede usar para el microscopio óptico o para el microscopio electrónico.
Esta técnica se basa en contrastar las muestras mediante una sustancia opaca en ambos microscopios. Ahora bien, para el microscopio óptico se contrasta la muestra a los fotones, mientras que en el microscopio electrónico se constrasta la muestra a los electrones.
Colorantes
Para el microscopio óptico, principalmente pueden ser dos:
- Tinta china.
- Nigrosina.
Tiñen el fondo de negro.
Preparación
El proceso de tinción consta de los siguientes pasos:
- Se hace una preparación en fresco de la muestra.
- Ahora se añade tinta china.
- Ya se puede observar
Si, de todas las tinciones, es el proceso más corto que hemos visto.
Utilidades
La principal función de la tinción negativa es observar las cápsulas bacterianas. Esto ocurre porque las cápsulas no absorben la tinta china, por lo que estas estructuras aparecen como zonas claras en un fondo negro, oscuro.
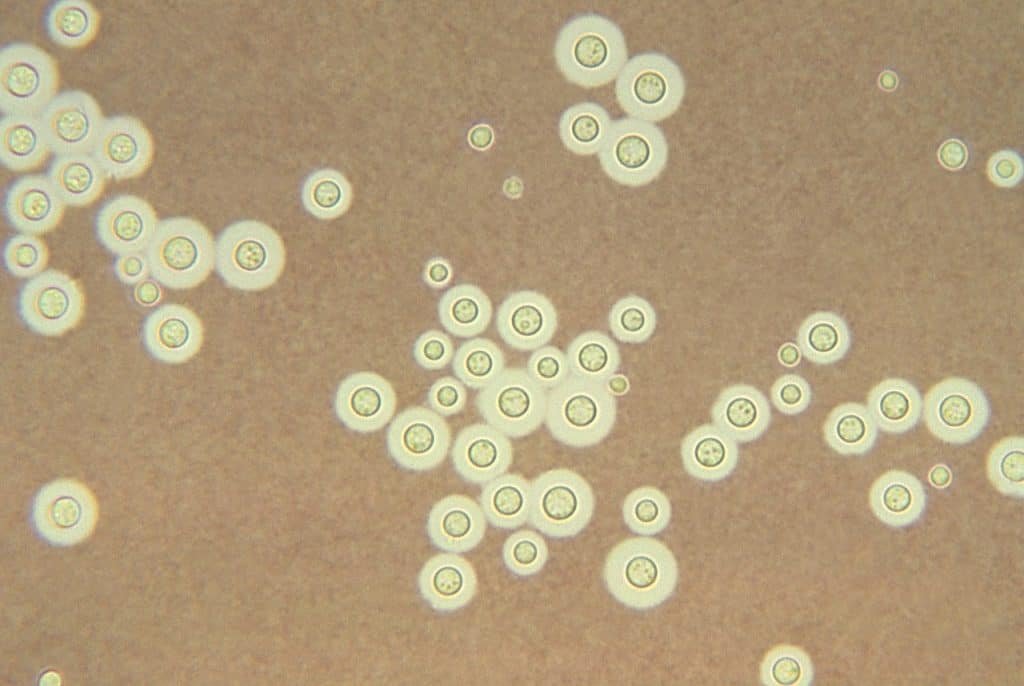
Ahora bien, se pueden añadir algún colorante de contraste para que las células bacterianas sean más visibles. Y, como ya hemos dicho, se puede usar nigrosina en vez de tinta china.
En el volumen V del Manual de Bergey se engloban 10 filos que no encajan en los grupos anteriores. Todas son GRAM negativas (-), pero existe gran variabilidad de morfología, fisiología y estilos de vida.
Índice de contenidos
Planctomyces
Bacteria acuática que tiene forma globular y posee un pedúnculo largo y estrecho al final del cual hay un disco adhesivo. A diferencia de otras pedunculadas, su pedúnculo no consiste en una extrusión citoplasmática con pared celular, sino que es de naturaleza proteica y se le califica como tallo. Sirve para adherirse a superficies o entre ellas.
Es una bacteria gemante con un ciclo de vida similar a las bacterias pedunculadas: con una fase nadadora y otra pedunculada. La forma nadadora se origina por gemación del cuerpo celular; se une a una superficie y comienza a formar un pedúnculo, que se va a ir alargando y, llegado un punto, genera una nueva célula por gemación.

.
Es quimioheterótrofa y anaerobia facultativa. Esta bacteria y sus relacionadas ocupan una posición filogenética específica, de forma independiente al resto. Carecen de peptidoglicano; su pared celular es proteica, de tipo capa S, rica en cisteína y prolina. Al no tener peptidoglicano, son resistentes a los antibióticos que actúan sobre este, como la penicilina. Por ello, para facilitar su aislamiento, se añade penicilina al medio.
Los planctomicetos poseen una compartimentalización interna, muy desarrollada, que incluye algo parecido a una estructura nuclear. Ciertos compartimentos carecen de DNA, y tienen otras funciones. Algunos parientes de Planctomyces son Gemmata y Brocadia anammoxidans.
El compartimento interno más grande es la membrana intracitoplasmática (ICM), separada de la membrana citoplasmática por una región libre de ribosomas denominada parifoplasma. Después de la ICM está el riboplasma. En el caso de Gemmata el nucleoide está dentro de una membrana del cuerpo nuclear; en Brocadia no ocurre esto, el compartimento más grande es el anamoxosoma, donde se realiza la reacción de anamox, y el DNA está fuera de la membrana del cuerpo nuclear.
Clamidias
Son parásitas intracelulares estrictas, es decir, deben crecer y multiplicarse dentro de células hospedadoras. Probablemente representan un paso más allá en la evolución en la pérdida de independencia; tienen menos funciones metabólicas propias que las rickettsias. Desarrollan una estrategia muy efectiva de supervivencia que incluye el parasitismo de los recursos del hospedador y la producción de una forma de resistencia para su transmisión. Están relacionadas con multitud de enfermedades y de síndromes.
Durante mucho tiempo fueron consideradas como formas intermedias entre los virus y las bacterias, por ser parásitos intracelulares, pero en realidad son bacterias ya que tienen DNA y RNA. Se pueden considerar las formas más simples de organización celular. Cuando entran en una célula hospedadora no pierden su integridad estructural, a diferencia de los virus. Son inmóviles, pequeñas y con un genoma de tan solo 4-6 x 108 Da.

Tipos de células
Tienen un ciclo vital que implica dos tipos de células: el cuerpo elemental (EB), que es la forma infecciosa, y el cuerpo reticulado (RB), que es la forma vegetativa.
El cuerpo elemental tiene forma de coco y no se multiplica, posee un material genómico electrón-denso y una pared celular rígida. Es relativamente resistente a ciertas condiciones adversas (desecación) y es la forma especializada en la dispersión; se transmite por el aire sin necesidad de vectores.
En cuanto al cuerpo reticulado, es la forma intracelular especializada en la división celular por fisión binaria. No es infecciosa. Tiene una forma algo más alargada y más grande que el cuerpo elemental. Posee un material genómico menos denso y contiene más ribosomas que el cuerpo elemental; y su pared es más flexible.
Aunque la envoltura de las clamidias se asemeja a la de otras GRAM negativas (-), no poseen peptidoglicano ni amino-azúcares semejantes. Poseen una capa P, proteica. Los EB alcanzan su estabilidad osmótica mediante enlaces cruzados entre proteínas de su membrana externa (CRP: proteínas ricas en cisteína), estableciendo puentes disulfuro entre estas cisteínas. También hay enlaces entre las proteínas periplasmáticas. Estos puentes disulfuro se reducen químicamente y son causa de la transformación de los cuerpos elementales a los reticulados.
Ciclo vital
Comienza con la fijación de un EB a la superficie de una célula hospedadora, que lo fagocita por endocitosis en lo que será el cuerpo de inclusión. La clamidia permanece dentro del endosoma y se reorganiza a cuerpo reticulado. Algún componente del cuerpo elemental inhibe la fusión del fagosoma al lisosoma; además, se producen cambios a nivel de la membrana del cuerpo de inclusión, permitiéndose la entrada de nutrientes del hospedador hacia la clamidia.
El cuerpo elemental se va transformando en cuerpo reticulado ya que va aumentando de tamaño, perdiendo rigidez de su pared, e inicia la síntesis de macromoléculas. Es probable que la síntesis inicial de RNA y proteínas vaya destinada a la producción de más ribosomas. Transcurridas de 8 a 10 horas, los cuerpos reticulados inician la fisión binaria, y tras 24-30 horas comienzan a transformarse en cuerpos elementales. Continúan el proceso hasta que la célula hospedadora se lisa (como en C. psittaci) y libera las clamidias o sale por un proceso de endocitosis inversa (como en C. pneumoniae).
Metabolismo
Su capacidad biosintética está más restringida que en el caso de rickettsias. De hecho, durante mucho tiempo se pensó que eran parásitos energéticos estrictos (necesitan robar ATP). No obstante, se ha comprobado, mediante la secuenciación de su genoma, que presentan genes implicados en la síntesis del ATP. No generan ATP porque poseen una translocasa de membrana del mismo tipo que el de las rickettsias, que pueden intercambiar ADP endógeno por ATP exógeno. Entonces, podemos decir que no son "parásitos energéticos estrictos".
Incluso, aunque carecen de peptidoglicano, presentan genes implicados en la síntesis de éste. Son sensibles a algunos antibióticos que inhiben la síntesis del peptidoglicano (ejemplo de pérdida evolutiva de función).
Cuando el hospedador aporta los precursores, los cuerpos reticulados pueden sintetizar sus propios componentes. Poseen porinas y proteínas de transporte activo de membrana, aunque se conoce poco de este transporte. Los cuerpos elementales poseen una actividad metabólica muy reducida, ya que están especializados en la dispersión.
Constituyen una rama independiente del dominio bacteria, aunque algo próxima a los planctomicetales. Hay dos géneros: Chlamydia y Chlamydophila.
Chlamydia
Desarrolla un solo cuerpo de inclusión, consecuencia de la fusión de los distintos endosomas formados por los diferentes cuerpos elementales que entran a la célula. En este cuerpo, Chlamydia retiene glucógeno como fuente de energía, y tiene un único operón ribosomal.
C. trachomatis es la especie más estudiada; posee muchos serotipos agrupados en 3 biotipos principales:
- Causante del tracoma. Infección crónica de la córnea y la conjuntiva y es el principal motivo de ceguera en el hombre. Causa dolor e inflamación.
- Causante del linfogranuloma venéreo: mucho más invasivo que el anterior, es una ETS. Causa también la uretritis no gonocócica. Afecta al tracto genitourinario, podemos calificarlo como el principal causante de las ETS más frecuentes.
- Afecta al ratón.
Chlamydophila
No acumula glucógeno y tiene 2 operones ribosomales.
- C. psittaci causa la psitacosis tanto en hombres como animales, considerada como una enfermedad epizoótica en aves, aunque también afecta a gatos, vacas, ovejas, etc. No sólo se transmite por contacto con las heces de los psitácidos, sino también de otras aves. Pude provocar diferentes tipos de infecciones gastrointestinales, afectación a la placenta, ojos, etc. Se contagia a través de la inhalación de los cuerpos elementales.
- C. pneumoniae puede provocar diferentes síndromes respiratorios en el hombre.
Espiroquetas
Las bacterias del filo Spirochaetes son gram negativas (-), quimioheterótrofas y poseen una morfología helicoidal, más o menos laxa dependiendo del género y especie. Son bastante delgadas y largas. Poseen el cuerpo cilíndrico, constituido por el protoplasma, y, a parte de la membrana, está rodeado por pared celular y una vaina (membrana externa), con 3 capas. El cuerpo cilíndrico es rígido, mientras que la vaina externa es flexible. La vaina rodea tanto al periplasma, la pared celular como al cuerpo cilíndrico. En el periplasma están los filamentos axiales.
El filamento axial rodea la espiroqueta y le permite el movimiento; está formado por fibrillas axiales conocidas como endoflagelos o flagelos periplásmicos, en número de 2 a más de 100, y están entre el peptidoglicano y la vaina (membrana externa). Se fijan cerca de los extremos celulares y se extienden hasta aproximadamente dos tercios de la longitud celular. Son rígidos y rotan unidos a cada extremo celular.
Como el cilindro protoplasmático también es rígido, al girar provocan en la vaina una onda o cresta helicoidal de tal manera que el cilindro protoplasmático gira en la dirección opuesta. Si está en contacto con alguna superficie el movimiento es de reptación. Si se daña o se elimina la vaina o filamento axial, la espiroqueta ya no puede moverse. Usan básicamente el mismo mecanismo de movimiento que otras bacterias, la rotación de flagelos rígidos adheridos a la membrana citoplasmática.

Están bien adaptadas a los medios viscosos que dificultan o impiden el movimiento por flagelos típicos. Esto explica por qué varias especies parásitas están restringidas a tejidos y fluidos animales.
Hay mucha variedad en cuanto a requerimiento de oxígeno: aerobias, anaerobias y anaerobias facultativas. Todas se dividen por fisión binaria.
El hábitat también es muy variado, aparecen tanto en ambientes acuáticos como terrestres, son frecuentes en lodos con materia orgánica en descomposición. Muchas son patógenas de hombre y animales.
Familia Spirochaetaceae
Spirochaeta
Es una bacteria acuática, inocua, de vida libre. Unas son anaerobias y otras son anaerobias facultativas. Junto con Cristispira es de tamaño muy superior a las demás, del orden de 2 a 40 filamentos axiales. Aparece en aguas dulces y marinas.
Cristispira
Es también acuática e inocua. Se considera comensal en el tracto digestivo de moluscos, aunque no se ha podido cultivar. Aparece exclusivamente en el estilo cristalino de moluscos, aunque no en todas las especies de moluscos. No se conoce la razón fisiológica de que aparezca en ese hábitat ni hay pruebas de que resulte nociva para su hospedador. Aparece más frecuentemente en moluscos sanos que enfermos. Tiene más de 100 fibrillas axiales en el filamento axial.
Treponema
Anaerobio con algunas especies microaerófilas. Hay especies comensales y otras patógenas: T. oralis y T. denticola son típicas de la boca, T. saccharophilum está presente en el rumen de rumiantes. T. pallidum causa la sífilis en el hombre. La vaina es muy delgada y son más pequeñas que las anteriores.
Borrelia
Es un género patógeno que suele usar vectores artrópodos. Tiene un cromosoma lineal y es de tamaño similar a Treponema.
B. recurrentis causa las fiebres recurrentes, que, si no tienen tratamiento pueden causar la muerte. Es una enfermedad sistémica debilitante que se transmite por un piojo.
B. burgdorferi causa la enfermedad de LYME, extendida en unas zonas de EEUU con una garrapata específica.
Familia Leptospiraceae
Son todas aerobias.
Leptospira
Es el género representativo, con dos especies.
- Dentro de Leptospira biflexa hay del orden de 60 serotipos y es de vida libre.
- L. interrogans es parásita patógena, con 218 serotipos establecidos, aunque que no todos afectan al hombre. El serotipo canicola no afecta al hombre, pero icterohaemorragiae sí. La enfermedad de Weil es causada en el hombre por el serotipo icterohaemorrhagiae, y a veces por el canicola. Esta enfermedad es una zoonosis que en ocasiones afecta al hombre. Se multiplica en diferentes partes del cuerpo y luego se pasa al hígado y riñones produciendo diversos daños, y puede contaminar por orina. Es de crecimiento lento. Utiliza como fuente de carbono ácidos grasos y alcoholes.
Acidobacterias
Forman parte del Phylum Acidobacteria. Es un grupo diverso (25 subgrupos) e importante por su amplia distribución en ambientes acuáticos y terrestres. Son las bacterias más abundantes del suelo.
Sólo se han podido cultivar unas pocas; de las restantes no se conoce tanto, sólo por estudios moleculares del SSU rRNA. Son muy abundantes en cuevas, del orden del 25% de la población de organismos presentes, además de ser las más abundantes de suelos ácidos.
De lo anterior podemos deducir que sí, son acidófilas. Algunas que son capaces de emplear el FeS están implicadas en la decoloración de objetos y obras de arte, así como de pinturas rupestres. Son GRAM negativos (-), quimioheterótrofas, de crecimiento muy lento. Tienen capacidades metabólicas variadas, unas respiran y otras fermentan; e incluso ejercen la fotosíntesis, como Chloroacidobacterium, que hace fotosíntesis anoxigénica. Es difícil inferir su papel en los ambientes donde se encuentran al ser tan abundantes.
Una de las que se ha podido cultivar es Acidobacterium, la cual es acidófila, aerobia y capsulada. Se ha aislado de aguas ácidas de drenaje minero. Usa tanto azúcares como ácidos orgánicos; algunas especies son anaerobias.
Bacteroidetes
El filo Bacteroidetes cuenta es bacilo gram negativo (-) anaerobio estricto, no formador de endosporas, cuyo género más representativo es Bacteroides. Es quimioheterótrofo, y fermenta azúcares y proteínas, y como producto se obtiene alguna mezcla de ácidos orgánicos (acetato y succinato).
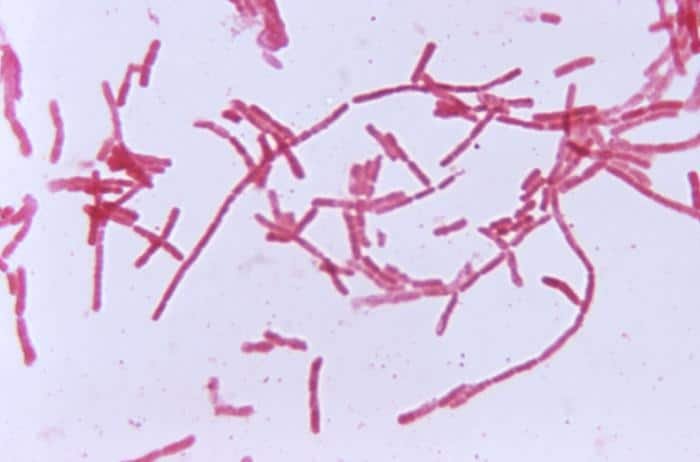
Son normalmente comensales en el tracto intestinal humano y de otros animales.
B. ruminicola aparece en el rumen de rumiantes. Son las más abundantes del intestino delgado del hombre. Algunas son patógenas; las anaerobias son las más importantes que están asociadas con infecciones humanas que pueden afectar desde el sistema nervioso central al sistema esquelético.
B. fragilis es muy frecuente en infecciones abdominales, pélvicas, pulmonares y sanguíneas.
Grupo Cytophagales
Son bacilos muy delgados, largos, GRAM(-) y a menudo, con los extremos puntiagudos, que se desplazan por deslizamiento. Están ampliamente distribuidas en agua y suelos donde pueden ser muy abundantes. Se enmarcan dentro del filo Bacteroidetes.
Sporocytophaga forma unas estructuras de latencia esféricas denominadas microcistos, similares a las bacterias nitrificantes. Junto con Cytophaga son aerobias, responsables de gran parte de la degradación bacteriana de celulosa en ambientes aerobios naturales.
Muchas degradan polisacáridos pero no mediante la secreción de enzimas extracelulares, sino por enzimas ligados a la pared celular. Esto explica por qué necesitan un contacto directo con las fibrillas de celulosa para degradarlas. También degradan quitina, queratina, pectina; incluso algunas marinas degradan el agar.
Desempeñan un papel muy importante en la mineralización de la materia orgánica y causan daños en aparejos de pesca y estructuras de madera expuestas. Aparecen en plantas de tratamiento de aguas residuales. Algunas son patógenas de peces como C. columnaris, que puede causar serios problemas en piscifactorías.
El movimiento parece que se debe a unas partículas esféricas de naturaleza proteica que rotan en el periplasma, a expensas del potencial de membrana o por gasto directo de ATP. Esto permite el deslizamiento de la célula a lo largo de las superficies.
Tiene una serie de ventajas:
- Hace que la bacteria entre en contacto con las fuentes de nutrientes insolubles, como celulosa o quitina
- Está bien adaptado a hábitats más secos y al movimiento dentro de masas sólidas como tierra, sedimentos, o madera podrida.
- Permite ubicar a la bacteria en las condiciones ambientales óptimas de densidad de luz, oxígeno, temperatura, etc.
Se consideran en conjunto a los géneros Rickettsia, Coxiella y Bartonella, ya que están encuadradas en el orden Rickettsiales y la familia Rickettsiaceae. Las rickettsias son un grupo heterogéneo de pequeños bacilos y cocobacilos GRAM negativos (-). Se desarrollan en el interior de la célula hospedadora, son parásitos intracelulares.
Índice de contenidos
Caracteres generales
Bartonella se encuentra evolutivamente cercana entre otros, de Rhizobium y Agrobacterium (relacionada con plantas), y esto ha dado a especular que las Rickettsias se originaron de bacterias que al principio eran infecciosas para plantas para ser después de animales.
Las Rickettsias tienen forma de coco o de bacilo o formas variadas (pleomórficas). Son todas proteobacterias GRAM negativas (-) e inmóviles. Coxiella y Rickettsia se consideran parásitos intracelulares estrictos; Bartonella se considera parásito intracelular pero facultativo. Crecen en eritrocitos, macrófagos y células del endotelio vascular de vertebrados, y a menudo también habitan en artrópodos que se alimentan de sangre: pulgas, garrapatas, piojos, entre otros; los cuales actúan como vectores u hospedadores primarios.
Tienen de particular el presentar una membrana permeable especial, por lo que son bastantes sensibles a la desecación. hace que su desecación sea bastante acusada y explica la necesidad de vectores de transmisión.
Hay una excepción en el caso de Coxiella, ya que podrá transmitirse a través del aire y a través de alimentos; no solo por vectores, gracias a que producen una forma de resistencia parecida a una endospora. Esto explica que además de poder sobrevivir en el aire, también resista la temperatura de pasteurización clásica (por eso hubo que elevar la temperatura) y el tratamiento con ciertos agentes antimicrobianos.
Parasitación
Entran en el hospedador mediante una fagocitosis inducida, que requiere que ambas partes (bacteria y hospedador) estén activos. Incluso ocurre en células que no son fagocíticas (células del endotelio vascular de vertebrados, por ejemplo). Cuando entran formarán un fagosoma (no rompen la membrana de la célula hospedadora).
En el caso de Rickettsia, entra por fagocitosis inducida formando un fagosoma; posteriormente degrada la membrana de ese fagosoma por medio de lipasas y es casi simultánea a la entrada por fagocitosis. Debido a esto, el fagosoma es casi indetectable, no constituye una fase intermedia. Fuera del fagosoma se dividen por fisión binaria, algunas especies se dividen en el núcleo y otras en el citoplasma. Finalmente, la célula hospedadora, dependiendo de la especie de Rickettsia, explota liberando la bacteria; en otros casos, se forman unas yemas que por contacto con la membrana permite finalmente la salida de las Rickettsias. Rompa o no la célula hospedadora, sufre daños debido al contacto tóxico de la pared celular de la Rickettsia con la pared de la célula hospedadora o por la rotura de la pared.
En el caso de Coxiella, entra por fagocitosis inducida, pero no se romperá la membrana del fagosoma, permaneciendo Coxiella en el fagosoma. Más tarde, se fusiona con el lisosoma, formando el fagolisosoma. Esta fusión es necesaria para activar el metabolismo de Coxiella, debido a que su metabolismo se acelera a pH 4,5 (pH del fagolisosoma), por lo que se multiplicará y saldrá lisando la célula.
Metabolismo
La Rickettsia respira glutamato o glutamina pero no degrada la glucosa. Esto parece proporcionarle sólo una pequeña cantidad de energía para el mantenimiento y no para el crecimiento; de ahí que sean parásitas intracelular. Tanto el glutamato como la glutamina la incorporan al ciclo TCA (en el intermediario α-cetoglutarato). Coxiella si respira glucosa, piruvato, etc. Bartonella respira ciertos ácidos orgánicos.
Tiene una cadena transportadora de electrones completa y obtienen el ATP por fosforilación oxidativa. Su capacidad biosintética es limitada, así que el resto de nutrientes los obtiene a partir de la célula hospedadora; para ello posee un sistema de intercambio de ADP endógeno por ATP exógeno (afecta a la célula hospedadora). Así, gran parte de la energía necesaria para el crecimiento se satisface por el metabolismo del propio hospedador.
El hecho de ser parásitas intracelulares las hace peculiares en cuanto al tratamiento con agentes quimioterápicos y antibióticos. Son resistentes a muchos antibióticos por desarrollarse en el interior del hospedador, pero pueden ser tratados con ciertos antibióticos como tetraciclinas o cloranfenicol. También son sensibles a las sulfamidas (Ejemplo: TMP-SMZ).
Suelen ser identificadas por pruebas serológicas.
En la siguiente tabla podemos ver las diferencias entre los 3 géneros de forma resumida.
| Bacteria | Rickettsia | Coxiella | Bartonella |
|---|---|---|---|
| Lugar de multiplicación | Citoplasma | Fagolisosoma | Superficie exterior de la célula |
| Parásito intracelular estricto | + | + | - |
| Puede cultivarse de forma axénica | - | - | + |
| Formación de esporas | - | + | - |
| Enfermedades humanas | Tifus, fiebre manchada de las Montañas Rocosas, etc | Fiebre Q | Fiebre de las trincheras |
Ahora lo veremos todo de forma más específica.
Rickettsia
Produce distintos tipos de tifus.
R. rickettssii
Produce la denominada "fiebre manchada de las Montañas Rocosas" que afecta a una zona de Norteamérica donde se encuentra el tipo de garrapata que es el vector de transmisión. Recibió el nombre en honor a Howard Taylor Ricketts (1871-1910), quien murió de tifus.
Ésta puede crecer tanto en el citoplasma como en el núcleo y usa una garrapata como vector. Puede que se transmita de generación en generación a través de los huevos por una transmisión transovárica o por garrapata-perro-humano.
Esta fiebre se caracteriza por cefaleas, escalofríos, aumento de la fiebre y un exantema (ronchas) cutáneo rojizo que comienza en muñecas y tobillos y después se extiende al tronco. Si no se trata puede afectar al corazón, pulmones y provocar incluso la muerte. Tiene tratamiento con antibióticos.
R. prowazeckii
Provoca el tifus exantemático o tifus epidémicos. Tiene una distribución mundial porque el vector que emplea es el piojo humano. Recibe el nombre de prowazekii en honor al Stanislav von Prowazek, que murió de tifus. Hoy en día hay tratamientos con antibióticos, además de una vacuna que se aplica a individuos de alto riesgo.
R. typhi (R. mooseri)
Provoca el "tifus endémico o murino". El nombre se le dio en honor a Herman Mooser que diferenció R. typhi de R. prowazekii. Se llama murino porque lo transmiten las pulgas de las ratas, las cuales pueden picar a las ratas o al hombre. Es una infección que puede permanecer indefinidamente en las ratas. La tasa de muerte es menor (<5%).
R. tsutsugamushi
Causa la fiebre fluvial japonesa o "scrub", y tiene una distribución oriental (Asia y Oceanía). El vector de transmisión es una garrapata que afecta a ratones de campo, que actúan de reservorio.
Coxiella
Coxiella burnetii
Causa la llamada "fiebre Q". El primero en investigarla fue Frank Mcfarlene Burnet y recibió el premio nobel en 1960. Se transmite por picadura a los animales de varias especies de garrapatas y estos animales infectados pueden parecer asintomáticos.

En el caso del hombre se suele transmitir por el aire, por inhalación de polvo contaminado por restos que contienen a estas bacterias, las cuales suelen estar en las heces, orina y leche de animales que están contaminados.
Después de inhalar ese polvo pasa a los pulmones donde prolifera y puede provocar inicialmente unos problemas respiratorios similares a la gripe y fiebre intensa. También puede provocar una endocarditis quellega a aparecer a los años desde la infección inicial. Durante todo ese tiempo lo normal es que permanezca en el hígado produciendo hepatitis.
La fiebre Q aparece normalmente en gente que trabaja en mataderos, granjas, etc. Se previene normalmente con vacunas en personas de alto riesgo, en zonas endémicas y pausterizando la leche.
Bartonella
Son bacilos curvados, pequeños y flagelados. Parasita células endoteliales y eritrocitos. A diferencia de las otras en las que hacía falta que el parásito y el hospedador tenían que estar activos, en Bartonella el hospedador (eritrocito) es pasivo, no contribuye a la entrada de las bacterias. Al entrar dañan su membrana, entra por endocitosis, pero no incita la fagocitosis como Coxiella y Rickettsia.
Es cultivada en condiciones axénicas en medio de una moderada complejidad. Entran gracias a los flagelos que poseen.
Bartonella quintana
Produce la "fiebre de las trincheras", (fiebre de los 5 días) que tuvo un gran impacto en la primera guerra mundial. Es una de las especies que no se desarrolla en el interior sino en la superficie externa, es decir, tienen una localización epicelular. Tiene una distribución mundial ya que el conductor es el piojo humano y el reservorio el hombre.
B. henselae
Produce la "enfermedad por arañazo de gato" (EAG). El vector es la pulga del gato y el gato es el reservorio. Estas sí viven dentro del eritrocito y el animal no muestra síntomas de la enfermedad. Causa fiebre e inflamación de los ganglios, que desaparece a lo largo de meses.
Otras proteobacterias
Agrobacterium
Son alfa-proteobacterias y están relacionadas con Rhizobium y Bartonella. Son bacilos con flagelación peritrica y además son fitopatógenos de dicotiledóneas como manzana, tomate, patata, etc. Algunas especies más destacadas son:
- A. rhizogenes. Causa raíces pilosas codificadas por un plásmido Ti.
- A. tumefaciens. Causa tumores en forma de agallas de corona localizadas en la zona de unión entre el tallo y la raíz, es decir, en el cuello. Esta transformación se produce cuando la bacteria transfiere un fragmento del plásmido Ti (tumor inducido) al material genético de la planta. Una vez inducida la agalla (tumor) puede seguir creciendo en ausencia de la propia bacteria. La formación del tumor se clasifica en 5 etapas.
Formación del tumor
Infección, reconocimiento y adherencia
Las células de A. tumefaciens se adhieren a las heridas de la planta, ya que estas heridas producen la liberación de compuestos fenólicos que las bacterias reconocen y que a la vez permiten la adherencia de ésta a la planta, activándose el proceso de transformación y formación de estos tumores. El reconocimiento bacteria-planta se produce por receptores.
El receptor vegetal es un tipo de pectina que es un polisacárido complejo que contiene y el receptor bacteriano tiene beta-glucanos que están incrustados o formando parte del lipopolisacárido de la pared celular de la bacteria. Tras ese reconocimiento, la bacteria sintetiza microfibrillas de celulosa para ayudarse a anclarse a la planta, formando unos grandes agregados bacterianos en la pared celular que facilitan la colonización.
Procesado del fragmento T-DNA del plásmido Ti
El plásmido Ti es bastante grande (unas 200 kb) pero contiene una región más pequeña denominada región T-DNA (unas 20kb) que es la que se transfiere al cromosoma vegetal. Dentro de la región T-DNA encontramos distintos genes que intervienen en la formación del tumor:
- Genes Onc (oncogenes): codifican enzimas que intervienen en la producción de fitohormonas, que estimulan la división celular y forman el tumor.
- Genes Ops (opinas): son genes que llevan la información genética para sintetizar opinas, que son aminoácidos modificados poco corrientes que emplea la bacteria como fuente de carbono y nitrógeno.
Dentro del plásmido Ti encontramos también distintos genes:
- Genes Vir (virulencia) que codifican proteínas esenciales para transmitir el fragmento T-DNA:
- Genes de transferencia (que codifican el puente conjugativo).
- Genes responsables de la degradación de opinas, para su posterior uso por la bacteria.
- Genes del sistema de doble componente.
La expresión de estos genes se induce por moléculas señal sintetizadas por los tejidos vegetales heridos como lo son ciertos compuestos fenólicos.
Transferencia del fragmento T-DNA por conjugación
Los compuestos fenólicos (sintetizados por los tejidos heridos de la planta) serán detectados por la bacteria, produciéndose un incremento de síntesis del gen VirA, el cual se adhiere a la membrana de la bacteria y actúa de sensor. A continuación VirA, como es una proteín-quinasa, activa por fosforilación al producto de VirG, que actúa de efector induciendo la transcripción de otros genes Vir al fosforilarse.
VirA y VirG constituten un sistema de dos componentes: se encuentran en procariotas superiores y en eucariotas y se emplean para la transmisión de señales al exterior. VirD codifica a una endonucleasa que va a cortar en una zona justo al lado de lo que se va a transferir (T-DNA). A continuación, actúa el producto de VirE, que es una proteína de unión que se une al lado de la cadena del DNA. Una vez cortado el T-DNA se une al fragmento y lo transporta a la célula vegetal. Finalmente, VirB forma el puente entre la bacteria y la célula vegetal para que se integre el T-DNA.
Integración del T-DNA en el genoma de la planta
Se integra en sitios con repeticiones en tándem específicas, inversas o directas.
Génesis de tumores y producción de opinas
El T-DNA codifica hormonas (opinas) para la planta que inducen la división de las células de la misma, produciendo un tumor. Presentan unos enzimas que permiten la catálisis de las opinas para su uso.
Tanto la bacteria como todos los procesos que lleva a cabo, han sido muy estudiados por su capacidad como vector en biotecnología de plantas. Así se han creado plantas transgénicas resistentes a determinados herbicidas o al ataque de determinados adversarios.
Brucella
Es una alfa-proteobacteria en forma de coco o bacilo e inmóvil. Es de interés clínico y es capaz de vivir frente a la fagocitosis. Pueden sobrevivir latentes meses o incluso años dentro de los fagocitos sin verse afectados por las defensas del organismo.
Es parásita intracelular facultativa. Causa la brucelosis en mamíferos, también llamada fiebre de malta o fiebres ondulantes.
Bordetella
Es una beta-proteobacteria en forma de bacilo pequeño e inmóvil. Las cepas virulentas tienen capsula, cuya formación está asociado con la toxicidad/ patogenicidad.
La más conocida es B. pertussis que causa la tos ferina. Esta especie solo afecta al hombre, y no soporta la fagocitosis. La tos ferina causa unos accesos paroxisticos de tos acompañados de una inspiración jadeante, similar a una especie de grito.
Francisella
Francisella que es una gamma-proteobacteria que cambian de forma dependiendo de la fase de crecimiento (bacilares en fases exponenciales y filamentosas en fase estacionaria), es decir, es pleomórfica. Son pequeños. Tiene una tinción de Gram bastante débil, aunque es GRAM(-).
Las cepas virulentas presentan capsula, y pueden sobrevivir a la fagocitosis. Es exigente y requiere medios complejos enriquecidos.
La más conocida es la F. tularensis (nombre que proviene del condado de Tulare, en California, donde se produjo la primera epidemia) que causa la tularemia. En realidad es una zoonosis propia de lagomorfos y roedores, pero que puede afectar al hombre y otros animales. Además presenta diferente sintomatología dependiendo de la vía de infección. Se puede adquirir por inhalación, ingestión, picadura de vectores artrópodos o a través de heridas, pero no de humano-humano. Provoca la inflamación de los ganglios linfáticos. Puede causar pneumonía, septicemia, abcesos (inflamación), etc. Es una bacteria que resiste meses a muy bajas temperaturas, bajo suelo, en plantas, agua, etc. Se le considera una posible arma biológica junto con Bacillus anthracis y Yersinia pestis (clasificados en el Grupo A por su virulencia, su resistencia y su gran infectividad).
Neisseria
Es otra beta-proteobacteria con forma de diplococo inmóvil. Algunos son capsulados (cápsula polisacárida en cepas virulentas). A veces presentan fimbrias que las usan para colonizar las mucosas.
Son aerobias estrictas y crecen a temperatura corporal. Algunas son inocuas (no causan problemas en el hombre) incluso algunas forman parte de la microbiota del hombre, pero otras son patógenas como N. gonorrhoeae (gonococo) que causa la gonorrea o N. meningitidis (meningococo) que causa la meningitis meningocócica.
Legionella
Es una gamma-proteobacteria. Tiene forma de bacilo con tendencia a ser filamentosos, móviles gracias a la presencia de flagelos polares o subpolares. También GRAM negativos (-) pero débiles porque se tiñen mal.
También sobrevive a la fagocitosis, de hecho inhibe la etapa de fusión del fagosoma con el lisosoma (para formar el fagolisosoma). Controla el transporte del fagosoma dentro del fagocito al retículo endoplasmático (RE) (orgánulo rico en nutrientes); dentro del retículo endoplasmático se multiplica y pasa desapercibido durante mucho tiempo dentro de este RE, asegurándose su supervivencia. Todas las especies de Legionella están implicadas como causa de neumonía en el hombre.

La especie tipo es L. pneumophila, que causa una neumonía denominada legionelosis. Es denominada así porque en 1976 muchos miembros de la legión americana murieron por una infección por esta bacteria. Tardaron en averiguar la causa de aquel brote de neumonía porque intentaban cultivar el agente en medios convencionales, pero necesita un medio rico (es nutricionalmente exigente).
Finalmente, lo identificaron al darse cuenta de que no crece en medios de cultivo habituales y que tiene mala tinción. Se aislaron a partir de cobayas infectadas con tejido procedente de pacientes infectados. Ya existen medios especiales de crecimiento para este microorganismo. Crecen en medios complejos enriquecidos, aunque tarda mucho en crecer.
Tiene tratamiento antibiótico y es un microorganismo que de forma natural se encuentra en aguas, pero no de forma libre sino que se encuentra en el interior de amebas que se pueden considerar como fagocitos naturales. Tiene facilidad para colonizar tuberías de suministro de agua caliente, sistemas de refrigeración de aires acondicionados.
En 2001 en Murcia hubo una epidemia, aunque hubo pocos fallecidos.
En general, las bacterias fotosintéticas son GRAM negativas. Están muy dispersas en el árbol filogenético. La mayoría de bacterias fotosintéticas son no proteobacterias, aunque algunas proteobacterias llevan a cabo el proceso de fototrofía también. En la siguiente lista se pueden ver su clasificación.
BACTERIAS FOTOSINTÉTICAS NO PROTEOBACTERIAS
- Fotótrofos oxigénicos
- Cianobacterias: Gloeothece, Synechococcus, Nostoc, Anabaena, Oscillatoria
- Proclorófitos: Prochloron
- Fotótrofos anoxigénicos
- Bacterias Verdes del azufre: Chlorobium
- Bacterias Verdes no del azufre: Chloroflexus
- Heliobacterias: Heliophillum
PROTEOBACTERIAS FOTOSINTÉTICAS
- Fotótrofos anoxigénicos
- Bacterias Rojas del azufre: Chromatium
- Bacterias Rojas no del azufre: Rhodospirillum
Índice de contenidos
Fotótrofos oxigénicos: Cianobacterias
Constituyen uno de los mayores Phylum de las bacterias. Su pared celular corresponde a una GRAM negativa (-). Fueron los primeros fotótrofos oxigénicos sobre la Tierra, quienes transformaron la atmosfera anóxica en óxica.

Llevan a cabo la fotosíntesis oxigénica y tienen fotosistemas I y II (PSI y PSII); como pigmento fotosintético poseen clorofila a situada en los tilacoides (que nada tienen que ver con los tilacoides de cloroplastos). También tienen unos pigmentos llamados ficobiliproteinas que actúan como pigmentos accesorios de antena; entre ellos se encuentran
- La ficocianina que confiere color azul y tiene una absorbancia máxima de 625 nm.
- La clorofila a que confiere color verde o verde-azulado.
- Algunas poseen ficoeritrina que da el color rojo con una absorbancia máxima de 550 nm y confieren también color marrón.
Por tanto, presentan un fenómeno de absorción cromática: si la bacteria crece con luz verde el contenido de ficoeritrina será mayor que el de ficocianina, y si crece con luz roja el contenido de ficocianina será mayor que el de ficoeritrina. Presentan diferente color dependiendo de la luz que incida sobre ellas.
Metabolismo
Las cianobacterias tienen una importante flexibilidad metabólica, lo que les otorga una gran diversidad: hay muchos tipos, se encuentran en muchos hábitats, con muchas formas de reproducción. El metabolismo mejor estudiado es el de los hidratos de carbono: tienen un ciclo de Krebs incompleto (les falta la α-cetoglutarato-deshidrogenasa) y hay un papel crucial de la ruta de las pentosas fosfato.
Todas son fotoautótrofas (salvo excepciones). Muchas son fotoautótrofas obligadas, y usan la vía más típica de fijación del CO2 (el ciclo de Calvin). Algunas pueden realizar fotosíntesis anoxigénica: pero en este caso, ya no pueden generar oxigeno, por lo que no pueden usar el agua como fuente de poder reductor. En este caso usan compuestos reducidos de azufre como donadores de electrones, y emplean solo el PSI. Obtienen el ATP mediante la fotofosforilación cíclica, depositando el azufre fuera.
Algunas realizan fotosíntesis anoxigénica, como las bacterias fotoheterótrofas y emplean la luz pero no fijan CO2 si disponen del compuesto adecuado. También las hay quimioheterótrofas aunque son pocas; estas aun estando en la oscuridad oxidan azúcares y crecen lentamente.
Organización celular
Hay cianobacterias unicelulares, de entre 1 y 10 µm, o son filamentosas. A dichos filamentos se les llama tricomas, y en ellos las bacterias están en contacto entre sí unas con otras por una amplia superficie. No se da movimiento por flagelos, salvo algunas excepciones que si presentan flagelos. Algunas tienen cápsulas mucilaginosas, lo que les permite movimiento por deslizamiento en contacto con una superficie. Las cianobacterias marinas presentan vacuolas de gas que usan para la flotación.
Tienen un hábitat muy variado: las cianobacterias pueden ser terrestres, acuáticas y simbiontes. Por ejemplo, Anabaena azollae, fijadora de nitrógeno, es endosimbionte de un helecho acuático llamado Azolla. Hay enorme variedad y diversidad:
- Synechococcus es responsable de un porcentaje significativo de CO2 fijado. Es pequeña, termófila y muy abundante en los océanos.
- Otras producen neurotoxinas (cianotoxinas) potentes que, cuando se acumulan en grandes cantidades, pueden causar muertes.
- Muchas son responsables del olor a tierra mojada, generado por las geosminas (producidas por los actinomicetos). Las cianobacterias también pueden producir geosminas.
Materiales de reserva
La principal reserva de carbono es el glucógeno. Algunas presentan, además, cianoficina como reserva de nitrógeno. Esta cianoficina está formada por arginina y asparragina (Arg-Asp) y alcanza hasta un 10% de la masa celular. También son un material de reserva los pigmentos de ficobilina en el heterociste, que son reservas de nitrógeno y contribuyen hasta un 10% de su masa celular.
Durante periodos de oscuridad pueden usar la cianoficina como fuente de energía, ya que la arginina puede hidrolizarse y producir ATP. Los pigmentos de ficobilina también pueden usarse como reserva de nitrógeno y constituir hasta el 10% de la masa celular, además de ser pigmentos accesorios de antena en la fotosíntesis.
En cuanto a la reproducción vegetativa puede ser por fisión binaria, gemación, fisión múltiple o fragmentación; esta última es típica de filamentosas que se dividen en hormogonios con vacuolas de gas que se separan del resto por deslizamiento. Su forma de resistencia son los acinetos característicos de algunas filamentosas. Son inmóviles y con pared celular engrosada. También pueden considerarse como forma de reproducción, ya que al germinar pueden generar nuevos filamentos vegetativos. Permiten a la cianobacteria protegerse de condiciones adversas (oscuridad, sequia, congelación, etc). Tienen una pared gruesa.
Fijación de nitrógeno
Fijación de nitrógeno. Las cianobacterias son las únicas que pueden realizar fotosíntesis oxigénica y a la vez poder fijar nitrógeno (por la enzima nitrogenasa, que es muy sensible al O2). Con pocas excepciones, las fijadoras de nitrógeno son las filamentosas y lo fijan en los heterocistes: células especializadas en la fijación, que se distribuyen de forma regular a lo largo del filamento o en los extremos, rodeadas por células vegetativas. No se crean en presencia de una fuente aprovechable de nitrógeno (para ahorrar energía y poder reductor).
Cuando van a sintetizar el heterociste producen una capa gruesa con una gran concentración de glucolípidos para evitar la difusión del oxígeno al interior celular, y dentro, se reorganizan las membranas fotosintéticas. Se destruye el fotosistema II para detener la producción de oxígeno. Tampoco presentan la enzima Rubisco, por tanto no fijan el CO2. Pero sí tienen fotosistema I por lo que sintetiza ATP, así que los heterocistes solo obtienen ATP, pero es dependiente de las células vegetativas vecinas para obtener el poder reductor.
Se sintetiza la nitrogenasa y se forman una serie de conexiones polares que comunican al heterociste con las células vecinas para intercambiar los productos de la fijación del nitrógeno con los productos de la fotosíntesis. Como producto de la fijación del nitrógeno destacan las glutaminas.
Si no hay heterocistes no se puede fijar nitrógeno a la vez que se realiza la fotosíntesis oxigénica. Sin embargo, hay algunas formas filamentosas que no tienen heterocistes pero pueden fijar nitrógeno siempre y cuando realicen fotosíntesis anoxigénica. Forman estructuras de resistencia llamados acinetos solo en algunas filamentosas.
Clasificación
Las cianobacterias se pueden clasificar en 5 grupos: 2 unicelulares y 3 filamentosas.
- Las unicelulares como Synechococcus y Gloeothece se dividen por fisión binaria. Gloeothece se rodea de una vaina que adhiere unas células con otras (engloba varias células) y fija nitrógeno en periodos de oscuridad.
- Otras unicelulares se dividen por fisión múltiple y pueden formar colonias. Algunas filamentosas como Anabaena y Nostoc presentan heterocistes. Anabaena no forma hormogonios; Nostoc sí. Algunas como Oscillatoria son filamentosas y no presentan heterocistes, pero sí fijan nitrógeno en las células del centro del filamento en las cuales no funciona el fotosistema II. Otras son filamentosas ramificadas.
Fotótrofos oxigénicos: Proclorófitos
Contienen clorofila a y b pero carecen de ficobilinas. La especie más representativa es Prochloron. Se parecen a eucariotas porque contienen clorofila a y a los cloroplastos porque tienen clorofila b.
Fotótrofos anoxigénicos: Bacterias verdes del Azufre
La especie representativa de este grupo es Chlorobium. Son bacilos GRAM negativos (-) e inmóviles. Algunas presentan vacuolas de gas, pero Chlorobium no.
El donador de electrones fotosintético es el H2S, formando azufre que depositan en el exterior de la célula (donde puede seguir siendo oxidado hasta sulfato). Emplean como pigmento fotosintético la bacterioclorofila (Bclorofila): Bclorofila a, además de Bclorofila c, d o e como pigmentos accesorios de antena. La antena se encuentra en los clorosomas. Tienen color verde o marrón en distintas tonalidades.
Desde el punto de vista fisiológico son fotoautótrofas anaerobias estrictas (no toleran el oxígeno). Fijan el CO2 por el ciclo TCA inverso. Viven en ambientes acuáticos anóxicos con abundante H2S y a mayores profundidades que cualquier otro organismo fotótrofo, ya que sus clorosomas son muy eficientes en la captación de luz y se necesita poca luz para la fotosíntesis.
Algunas forman asociaciones en parejas de bacterias quimioheterótrofas llamadas consorcios donde las dos bacterias salen beneficiadas. En estas asociaciones existe un epibionte que es fotótrofo y una célula quimioheterótrofa.
Se sabe que tiene que haber algún tipo de comunicación entre ambos organismos ya que sincronizan sus divisiones celulares, aunque aún no está claro el mecanismo de adhesión. Los quimioheterótrofos pueden ayudarlos a moverse (trasladarlos a una zona adecuada para realizar la fotosíntesis). Además, pueden recibir nutrientes orgánicos procedentes de los fotótrofos.
Fotótrofos anoxigénicos: Bacterias verdes No del Azufre
La especie más representativa es Chloroflexus. Hay muy poca diversidad. Son bacterias GRAM negativas (-), filamentosas, deslizantes y termófilas.
Se consideran fotótrofos "híbridos" porque tienen un mecanismo fotosintético con bacterioclorofila c y clorosomas, al igual que las bacterias verdes del azufre, pero tienen bacterioclorofila a y obtienen el poder reductor por transporte inverso de electrones (como las bacterias rojas), aun cuando las verdes no suelen necesitarlo. Tienen un fotosistema que se parece al de las bacterias rojas, y por ello necesitan ese transporte inverso. Se considera un descendiente de fotótrofos primitivos.
Sobre su fisiología podemos decir que, en ausencia de oxígeno, crece mejor como fotoheterótrofo. No obstante, puede crecer como fotoautótrofo por la vía del hidroxipropionato (autotrofía). En la oscuridad, puede vivir actuando como quimioheterótrofo llevando a cabo incluso respiración aerobia. Tienen mayor diversidad metabólica que las bacterias verdes del azufre. Viven en manantiales neutros o alcalinos formando gruesos tapices bacterianos (junto a cianobacterias).
Fotótrofos anoxigénicos: Bacterias Rojas
Son proteobacterias GRAM negativas (-). Es un grupo muy amplio; pueden estar clasificadas según criterios filogenéticos, morfológicos y fisiológicos. Son morfológicamente muy diversos.
Realizan fotosíntesis anoxigénica. Poseen como pigmentos fotosintéticos Bclorofila (a, b) y carotenoides como pigmentos accesorios de antena, que dan color púrpura, rojo o marrón. Se sitúan en invaginaciones de la membrana citoplasmática; así aumenta la superficie y pueden tener más cantidad de pigmentos para aprovechar mejor la luz. Cuando hay luz intensa se reduce la cantidad de membranas y pigmentos. Presentan autotrofía, fijando CO2 mediante el ciclo de Calvin.
Los diferentes géneros de las bacterias rojas están dentro de distintas clases: alfa, beta y gamma. Pueden ser:
Del azufre
Son γ-protebacterias (gamma), y la especie más representativa es Chromatium. Se denominan del azufre porque emplean como fuente de poder reductor compuestos reducidos del azufre: oxidan S2- (S2O32-) y producen S0 que NO va a ser depositado en el exterior de la célula, sino que lo mantienen dentro formando glóbulos refringentes (acumulaciones de azufre). Son anaerobias estrictas con fotosíntesis anoxigénica.
Habitan en zonas acuáticas anóxicas iluminadas con abundante H2S; por ejemplo, lagos meromícticos y manantiales sulfurosos. Los lagos más adecuados son los llamados lagos meromícticos, que son lagos permanentemente estratificados, ya que tienen agua más densa (salada) en el fondo y menos densa (dulce) más cerca de la superficie.
Si existe suficiente sulfato por permitir su reducción, el sulfuro producido en los sedimentos puede difundir desde las zonas anóxicas y es ahí donde las bacterias rojas se podrán desarrollar formando masas densas celulares.
No del azufre
Son α (alfa) y β-proteobacterias (beta), y la especie más representativa es Rhodospirillum. Constituyen un grupo muy amplio y heterogéneo. Se denominan no del azufre porque en principio se pensó que no podían usar el azufre como fuente poder reductor. Sin ambargo, sí pueden oxidarlo en bajas concentraciones.
Su éxito competitivo radica en la capacidad de realizar fotosíntesis, pero siendo fotoheterótrofas (es decir, no fijando el CO2). Son fotoheterótrofas o raramente fotoautótrofas en ausencia de oxígeno. Para realizar fotosíntesis siempre necesitan condiciones anóxicas. Como compuesto orgánico usan azúcares, alcoholes, etc. Tienen gran diversidad de sustancias nutricionales.
La mayoría también pueden crecer como fotoautótrofas que fijan el CO2 por el ciclo de Calvin, eso sí, si no hay oxígeno en el medio. También pueden vivir en la oscuridad, y son quimioheterótrofas que realizan respiración anaerobia, respiración aerobia y fermentación. Pueden crecer en presencia de oxigeno siempre y cuando no haya luz. Pueden llegar a ser quimiolitótrofas en ausencia o presencia de oxígeno. Algunas incluso pueden usar el hidrógeno como fuente de poder reductor.
Fotótrofos anoxigénicos: Heliobacterias
Son GRAM positivas (+), aunque se tiñen muy mal por su bajo contenido en peptidoglicano. Filogenéticamente están relacionadas con Clostridium, ya que ambos forman endosporas y contienen dipicolonato cálcico y siempre fermentan. Hay pocos géneros.
Son bacilos largos o cortos con extremos puntiagudos y móviles, ya sea por flagelos o por deslizamiento. En Heliophylum, las células se van agrupando y se mueven como una unidad. Son anaerobias estrictas. Realizan fotosíntesis anoxigénica, y para ello poseen una forma exclusiva de Bclorofila: la bacterioclorofila g.
En cuanto a su fisiología, son fotoheterótrofas en ausencia de oxígeno. En la oscuridad, son quimioheterótrofas solo en ausencia de oxígeno y llevan a cabo fermentación; por eso se asemejan al género Clostridium. Viven en el suelo (arrozales) donde su actividad como fijadoras del nitrógeno puede beneficiar a las plantas del arroz. Los cambios de temperatura y humedad las relacionan con el género Clostridium. También se las ha encontrado en ambientes muy alcalinos (lagos y suelos).
La observación microscópica es crucial en microbiología, permitiendo el estudio detallado de microorganismos. La evolución de los microscopios ha transformado esta disciplina, facilitando la identificación y caracterización de diversas especies.
Además, el uso de diferentes técnicas de tinción ha ampliado las posibilidades de análisis, permitiendo resaltar características morfológicas y estructurales que serían difíciles de apreciar sin estos métodos.
Índice de contenidos
Técnicas de observación microscópica
La microbiología esta indudablemente unida al progreso de los microscopios. De hecho, la historia de la microbiología como ciencia comienza con la creación de microscopios. Para observar mejor a los microorganismos se han desarrollado colorantes, tinciones diferentes que se usarán en función de nuestro objetivo.
Microscopios
Un microscopio es un conjunto de lentes que concentran y enfocan la luz sobre una muestra para formar imágenes visuales. El concepto de microscopio se basa en una propiedad física de la luz: la difracción. Cuando un rayo de luz pasa por dos superficies distintas, que produce una desviación que produce un retraso en la velocidad conocido como índice de refracción, producido entre dos medios cuando la luz pasa a través de ellos.
Fundamentos de microscopía óptica
- Ampliación o aumento. Número de veces que aparece resaltado el tamaño de un objeto y que es el producto de la lente ocular por la objetiva.
- Contraste. Diferencia de intensidad lumínica que hay entre la muestra y el medio. Para aumentar el contraste se recurre a medios de tinción.
- Poder de resolución (PR). Depende de:
- La longitud de onda (λ) de la luz visible usada (entre 0.4 y 0.7 µm)
- La apertura númerica (AN). Es igual a n*sen θ donde
- n. Es el índice de refracción del medio que atraviesa el haz, entre el cubreobjetos y el objetivo. Su valor es:
- 1. En el aire.
- 1.33. En agua.
- 1.5. En aceite de inmersión.
- θ. Es la mitad del ángulo del cono de luz que entra al objetivo desde la muestra.
- n. Es el índice de refracción del medio que atraviesa el haz, entre el cubreobjetos y el objetivo. Su valor es:
- Límite de resolución (LR). Es la distancia mínima que debe existir entre dos puntos para poder diferenciarlos como tales. La ecuación sería esta:
LR = λ / (2n * sen θ)
Con los microscopios normales no se puede observar a menos de 100nm; el objetivo máximo en un microscopio óptico es 100x (solo usando el aceite de inmersión, sino 50x).
Tipos de microscopios
- Microscopio de campo claro. Las muestras se visualizan al destacar sobre un fondo iluminado. Se puede aumentar el contraste sin necesidad de teñir. El contraste entre muestra y medio es muy pobre.

- Microscopio de fondo oscuro. Normalmente en las muestras el contraste entre la célula viva y el agua es muy difícil de resolver con un microscopio de campo claro. Pero este microscopio cambia las condiciones. Se coloca un condensador especial que impide el acceso de luz a la muestra directamente y sólo los rayos oblicuos que inciden son reflejados. Se enfoca un cono hueco de luz sobre la muestra, de modo que sólo la luz reflejada o refractada por la muestra puede formar una imagen. Se observa una imagen con un fondo oscuro y los rayos oblicuos hacen que la muestra se vea iluminada o brillante. Se usa para visualizar microorganismos que son difíciles de teñir por sus características o no se ven con el microscopio normal. Organismos frágiles o que se tiñen muy mal. Ejemplos: La bacteria de la sífilis (Treponema palium) o las espiroquetas que son muy delgadas.
- Microscopía de contraste de fases. Permite visualizar células sin necesidad de tinción. El condensador tiene un diafragma anular que produce un cono hueco de luz, y un objetivo con anillo de fase en una placa cambiadora de fase. Las células tienen un índice de refracción (n) distinto al del medio y desvían los rayos de luz que las atraviesan. La luz que pasa a través de una muestra sufre un retardo. A lo largo del microscopio se intercalan uno o más anillos de fase, que hacen pequeños retrasos en la refracción de la luz cuando pasa de un medio a otro, y los amplifica. Hay dos tipos de luz: la directa y la en fase (retardada). Cuando los dos tipos se integran en el ocular, forman una imagen muy contrastada con áreas muy iluminadas (en fase) y otras muy oscuras (fuera de fase), que va a permitir visualizar la morfología y tamaño de células y composición citoplasmática, Phb, gránulos de volutina, si hay endosporas en formación. Estos componentes no se observan de ninguna otra manera.
- Microscopio de interferencia diferencial. Este microscopio crea una imagen sobre la base de la detección de diferencias entre los n y el espesor de la muestra. Unos prismas generan dos ondas de luz polarizada plana en ángulo recto, una respecto de la otra. Una de las ondas pasa a través de la muestra, y la otra sirve de referencia, y pasa por una zona clara. Tras atravesar la muestra, las dos ondas se combinan e interfieren entre sí; llegan desfasadas al ojo y forman una imagen tridimensional. Si no hay muestra los dos haces llegan al mismo tiempo. Así, diversas estructuras aparecen claramente visibles, tales como paredes celulares, endosporas, gránulos, vacuolas y el núcleo de células eucariotas.
- Microscopio de luz UV. Utiliza una longitud de onda que está en el ultra violeta (200-300nm).
- Microscopio confocal. Usa como fuente de luz los rayos láser. Las muestras se marcan son fluorocromos en general. El rayo láser se dispone en todos los planos de la partícula, va analizando la muestra en distintos planos, y los superpone creándose un registro tridimiensional.
- Microscopía de fluorescencia. Consiste en detectar en la muestra qué emite luz, ya que ciertas moléculas y estructuras son fluorescentes y se excitan con energía radiante. Parte de esa energía que emiten es detectada por el microscopio (por ejemplo, la clorofila, que tienen sustancias fluorescentes naturales). En otras ocasiones se necesita marcar dichas estructuras o moléculas con fluorocromos, tales como la rodamina B o isotiocianato de fluoresceína para poder localizarlas. Un filtro excitador permite pasar la radiación excitada de la longitud de onda (λ) deseada, que es reflejada por el filtro dicroico, y enfocada por la lente del objetivo sobre la muestra. Las móleculas fluorescentes de la muestra se excitan y emiten luz de λ específica y mayor. Esta luz es enfocada por el objetivo y la mayor parte pasa a través del filtro dicroico y no se refleja. Un filtro de barrera final bloquea la luz residual con la frecuencia de la luz de exitación. Su aplicación es en especial en microbiología médica y ecología microbiana.
- Microscopio de fuerza atómica (AFM). Se fundamenta en las interacciones atómicas de las partículas de la muestra que son captadas por un dispositivo situtado muy cerca de la muestra. Se trata de una sonda que se va moviendo sobre la muestra y recoge datos de las repulsiones atómicas (ondas desprendidas). Todo lo que detecta el dispositivo se transmite a través de un sistema informático, y en una pantalla se muestran los resultados tridimensionales.
- Microscopía electrónica. Usa una corriente de electrones que se desplaazan a través de unos lentes electromagnéticos y se van a proyectar sobre una muestra extremadamente fina que tiene que estar en condiciones de vacio extremo.
- Microscopio electrónico de transmisión (MET). Se puede aumentar el contraste mediante la tinción negativa, o los métodos de sombrado o criofractura.
- Microscopio electrónico de barrida (MEB). Útil para ver estructuras en 3 dimensiones.
Microscopio óptico vs Microscopio electrónico
En la siguiente tabla se pueden ver las diferencias entre el microscopio óptico y el microscopio electrónico.
| MO | ME | |
| Aumento | 1.000-1.500 | > 100.000 |
| Resolución máxima | 0,2 µm | 0,5 nm |
| Fuente de radiación | Luz visible | Haces de electrones |
| Lentes | Lentes de vidrio | Lentes electromagnéticas colocadas simétricamente respecto al eje axial que enfocan el haz de electrones, a través de un tubo en el que se ha hecho vacío, sobre la muestra. |
| Fuente de contraste | Absorción de luz diferencial | Dispersión de electrones |
| Medio de desplazamiento | Aire | Alto vacío |
| Montaje de la muestra | Portaobjetos | Rejillas metálicas Tratamiento previo de las muestras |
Observación de microorganismos. Preparaciones
Basicamente, se pueden observar a los microbios mediante 2 tipos de preparaciones:
- Preparación húmeda o fresca. En esta se observan los microorganismos vivos. Es típica de los microscopios de campo oscuro y de contraste de fases. Se usa en caso de que la morfología se altere al usar alguna tinción. Sirve para determinar la movilidad u observar cambios citológicos o algunas inclusiones.
- Preparación teñida. Permite ver a los microorganismos en función de su capacidad para retener o no determinados colorantes. La principal ventaja es que aumenta el contraste, acentuando las características morfológicas pero conservandolas. Los colorantes se usan para formar las tinciones.
Colorantes. Tinciones
Para mejorar el contraste entre los microorganismos y el medio lo que hlacemos es recurrir a las tinciones, tratando las muestras celulares mediante colorantes que son sustancias con una afinidad especial por determinados componentes o estructuras celulares. Como resultado de la tinción lo que vamos a observar son muuestras de microorganismos teñidas más contrastadas sobre un medio difuso (no teñido). En microbiología vamos a utilizar siempre preparaciones fijadas, es decir, muestras de células muertas, y para las tinciones se utilizan colorantes (no tintes).c
Todo colorante lleva dos partes:
- Grupo cromóforo. Parte de la molécula responsable del color, es el radical cromóforo. Se trata de moléculas alifáticas que suelen llevar un doble enlace conjugado (N=N) o un grupo sulfo (SO2).
- Grupo auxocromo. Región de la molécula que no tiñe pero que facilita la interacción del radical cromóforo con la molécula que va a teñir. Suelen ser radicales iónicos (OH–, COO–, NH2+) muy activos con capacidad para interactuar.
Los colorantes se van a clasificar en función del grupo auxocromo:
- Grupo auxocromo ácido o aniónico (-). El grupo auxocromo es un anión y va a interaccionar con componentes celulares básicos de la célula, como el citoplasma y estructuras con carga positiva. Ejemplos: eosina, rojo-congo, fucsina, nigrosina.
- Grupo auxocromo básico o catiónico (+). El grupo auxocromo es un catión y va a interaccionar con regiones o zonas ácidas de la célula que tengan carga negativa, como con los ácidos nucleicos. En general todas las bacterias tienen una carga externa negativa: estos colorantes van a interaccionar sobre todo con la pared bacteriana. Ejemplo: safranina, azul de metileno, cristal violeta.
- Grupo auxocromo sin carga, liposoluble. Combinación de un anión y un catión que normalmente en solución para teñir se van a disociar en los dos átomos. Ejemplo: eosina de metileno, negro-sudán.
Fases de la tinción
Comprende varias partes:
- Extensión. Se toma la muestra y se extiende a lo largo del porta.
- Secado breve.
- Fijación. Normalmente se fijan suavemente con una llama, y es una fijación en un doble sentido: una fijación física que consiste en que la capa que hemos puesto quede pegada al cristal y una fijación biológica, de tal manera que cuando se aplica calor se desnaturalizan las estructuras celulares, se coagulan las proteínas en su conformación nativa de manera que ahora puedan tomar el colorante. Solo en algunos casos se puede acudir a una fijación química.
- Aplicación del colorante. Es el proceso de tinción en si mismo.
- Lavado.
- Observación.
Mecanismos de tinción
Fundamentalmente hay dos:
- Tinción por intercambio iónico. Si tenemos una bacteria con carga negativa y le añadimos azul de metileno, el grupo auxocromo desplaza a los cationes adheridos a la pared bacteriana y los sustituyen, liberándose cloruro sódico.
- Tinción por solubilidad diferencial del colorante entre la muestra y el medio. Las células en un medio acuoso tienen estructuras hidrofóbicas en su interior. Si teñimos con negro-sudán (que es lipofílico) no se disuelve en el agua y se une a las regiones hidrofóbicas (o con un alto contenido en lípidos), y así tiñe.
Tipos de tinciones
- Simple. Aplica un único colorante que tiñe completamente las células. Normalmente es con azul de metileno. No es muy útil (se obtiene información sobre la forma y variedad, pero poco mas).
- Diferencial. Incorpora 2 colorantes de forma excluyente (cada bacteria se teñirá con uno de ellos, pero no con los dos). Tinción de GRAM (1884) y tinción de Ziehl-Neelsen (para las bacterias acido-acohol resistentes).
- Específica o selectiva. El colorante se adhiere y tiñe determinadas estructuras especificas de la célula por las que tiene afinidad. Endosporas, volutinas, flagelos. Leifson, con rosanilina (que tiene acido tánico), aumenta la visibilidad del flagelo, que se fija con formol. Como ejemplos tenemos la tinción negativa, la de flagelos, o endosporas.
En el artículo que enlazamos a continuación podrás ver las tinciones y colorantes principales usados en microbiología.
Tinción de Gram
Data del año 1884, por Hans Christian Gram. La preparación consta de varias partes:
- Se prepara el frotis, y se tiñe en primer lugar con cristal violeta (generalmente durante 1min, aunque el tiempo depende de la pureza del colorante). TODAS las células se tiñen de color azul violeta.
- Se añade lugol, que es una solución de Iodo y ioduro potásico que tiene función de mordiente es decir se une con el cristal violeta y forma un complejo insoluble que queda atrapado y absorbido dentro de las células.
- Esta es la etapa crítica: decolorar con alcohol de 96º. Todas las células toman el primer colorante pero cuando le añadimos el alcohol, las GRAM- pierden el colorante, mientras que las GRAM+ siguen coloreadas.
- Ahora añadimos el colorante de contraste, en este caso, la safranina, la cual tiene que tener un grupo cromóforo que no sea violeta, que suele ser rojo rosa. Ahora las GRAM+ se ven color violeta y las GRAM- de color rosa.
Es preferible utilizar cultivos jóvenes, para evitar alteraciones en la pared y por lo tanto, confusiones. Si se abusa del alcohol se puede extraer la tinción de las GRAM+ por lo que hay que tener cuidado.
Para ver la tinción de Gram con más detalle tienes el siguiente artículo donde se analiza la tinción de Gram además de otras tinciones y colorantes usados en microbiología.
¿Alguna vez te has preguntado cómo las bacterias logran mantener su forma y protegerse a sí mismas contra factores externos? La respuesta está en el peptidoglicano, una molécula clave en la estructura de la pared celular de las bacterias.
Este material es tan importante para ellas, que sin él simplemente se desintegrarían. ¿Quieres saber más sobre cómo el peptidoglicano juega un papel crucial en la biología bacteriana? ¡Sigue leyendo para descubrirlo!
Índice de contenidos
Qué es el peptidoglicano
El peptidoglicano es un compuesto exclusivo de bacterias, formado por azúcares y aminoácidos, de ahí su nombre (péptido, uno o más aminoácidos unidos mediante enlaces químicos; glicano, polímero de monosacáridos, o, en otras palabras, conjunto de azúcares simples). No es una proteína.
Es el compuesto cuya función es dar rigidez, consistencia y forma a la pared celular bacteriana. De hecho, si se inhibe su biosíntesis o su degradación especifica durante el crecimiento celular esto acaba provocando la lisis celular; de ahí que muchos antibióticos ataquen estos procesos.
La pared celular es un elemento de suma importancia en la bacteria, ya que resiste la gran presión osmótica interna de la célula, y el peptidoglicano es el elemento clave para sus características. La composición química de esta compuesto es bastante similar en GRAM+ y GRAM-, aunque tienen diferencias que veremos más adelante. De hecho, esas diferencias son las que dividen a las bacterias en estos dos grupos: bacterias gram positivas y gram negativas. El peptidoglicano también se conoce como peptidoglucano o mureína. Es un compuesto que aparece exclusivamente en bacterias; no aparece en organismos eucariotas.
La cubierta de peptidoglicano envuelve a la célula bacteriana, y se encuentra por encima de la membrana celular, pero debajo de la membrana externa en las bacterias que tengan esta estructura (bacterias GRAM negativas).
Composición. ¿De qué está hecho el peptidoglicano?
El peptidoglicano está formado por una secuencia alternante de dos azúcares, N-acetil-glucosamina (NAG) y el ácido N-acetilmurámico (NAM), unidos por enlaces β(1→4), entre el C1 de NAM y el C4 de NAG*. NAM es un derivado de NAG al que se le ha añadido una molécula de ácido láctico en el C3. La estructura del peptidoglicano está conformada por tres capas que veremos a continuación.
*En el caso de las arqueas, su pared celular tiene pseudopeptidoglucano formado por N-acetil-glucosamina unida a N-acetiltalosaminomurámico mediante enlaces β(1→3).
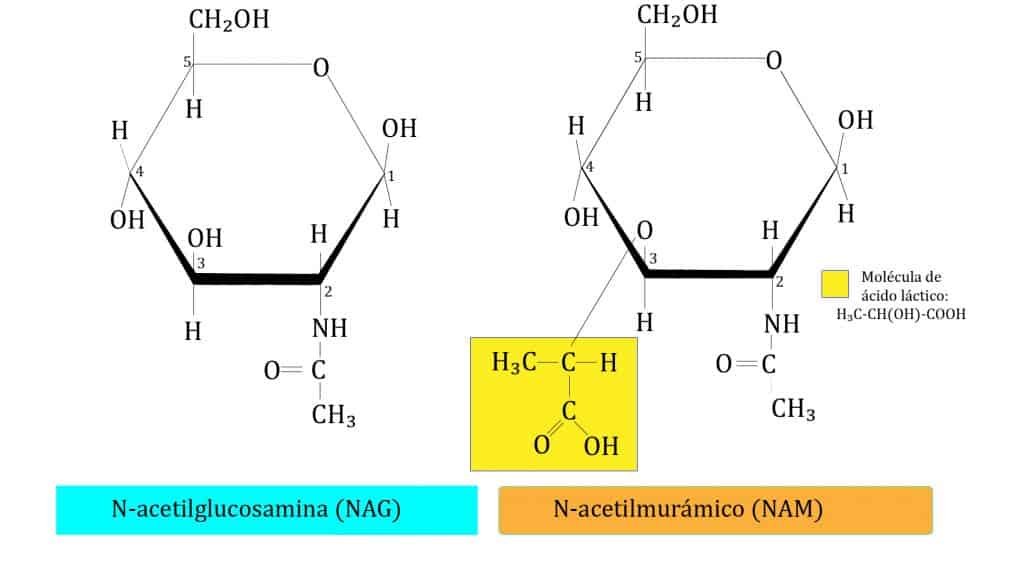
La primera capa del peptidoglicano (horizontal) está formada por filas lineales de NAG y NAM unidos de forma secuencial, mediante enlaces covalentes.
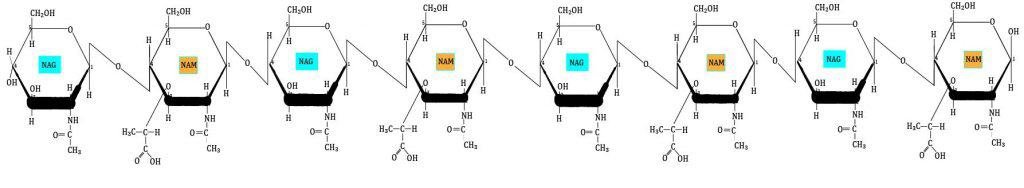
La segunda capa (vertical) está formada por un tetrapéptido unido solamente a NAM (esta es otra diferencia entre NAG y NAM). A este tetrapéptido se le denomina tetrapéptido del glicano. Este tetrapéptido contiene:
- L-alanina
- D-glutámico (en algunas bacterias puede estar hidroxilado)
- L-lisina en la mayoría de GRAM+ o meso-diamino-pimélico (m-DAP) en GRAM- y algunas GRAM+ (en GRAM+ también pueden aparecer otros aminoácidos)
- D-alanina
La formulación de estos aminoácidos unidos a NAM se encuentran en la imagen de abajo.
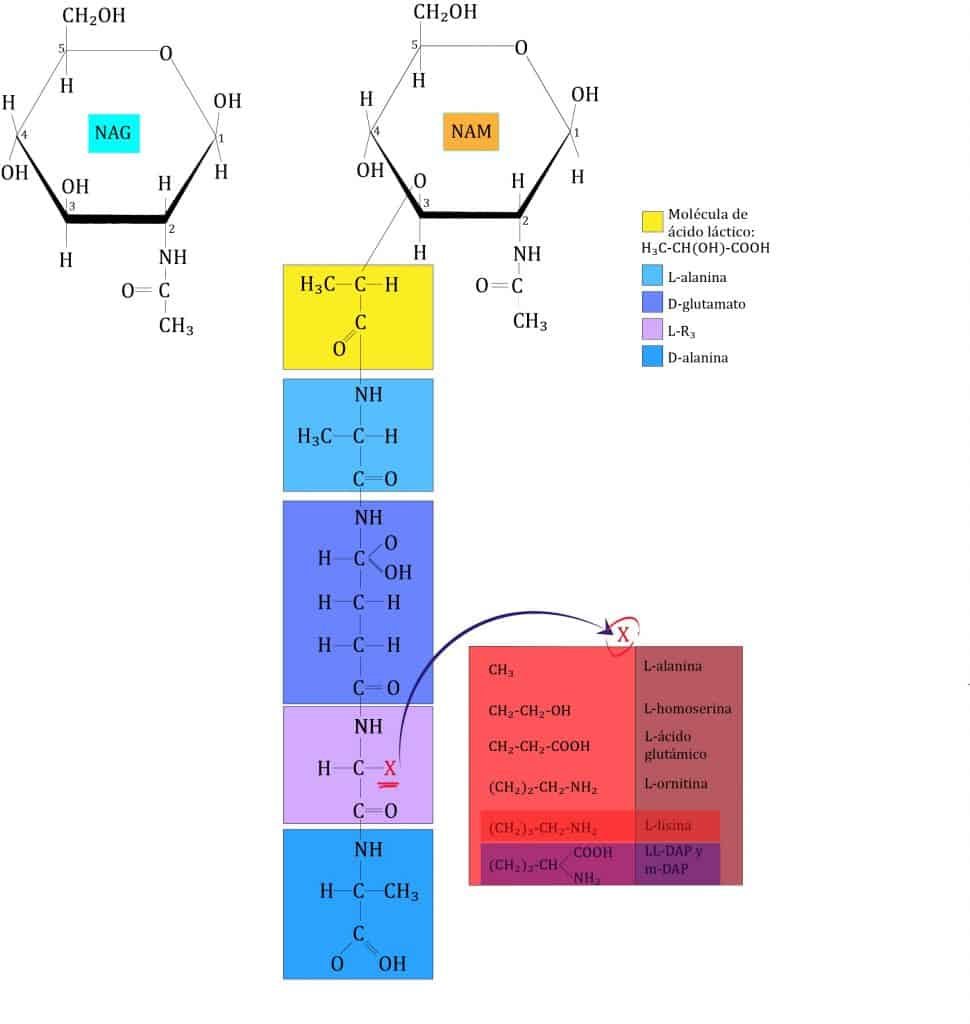
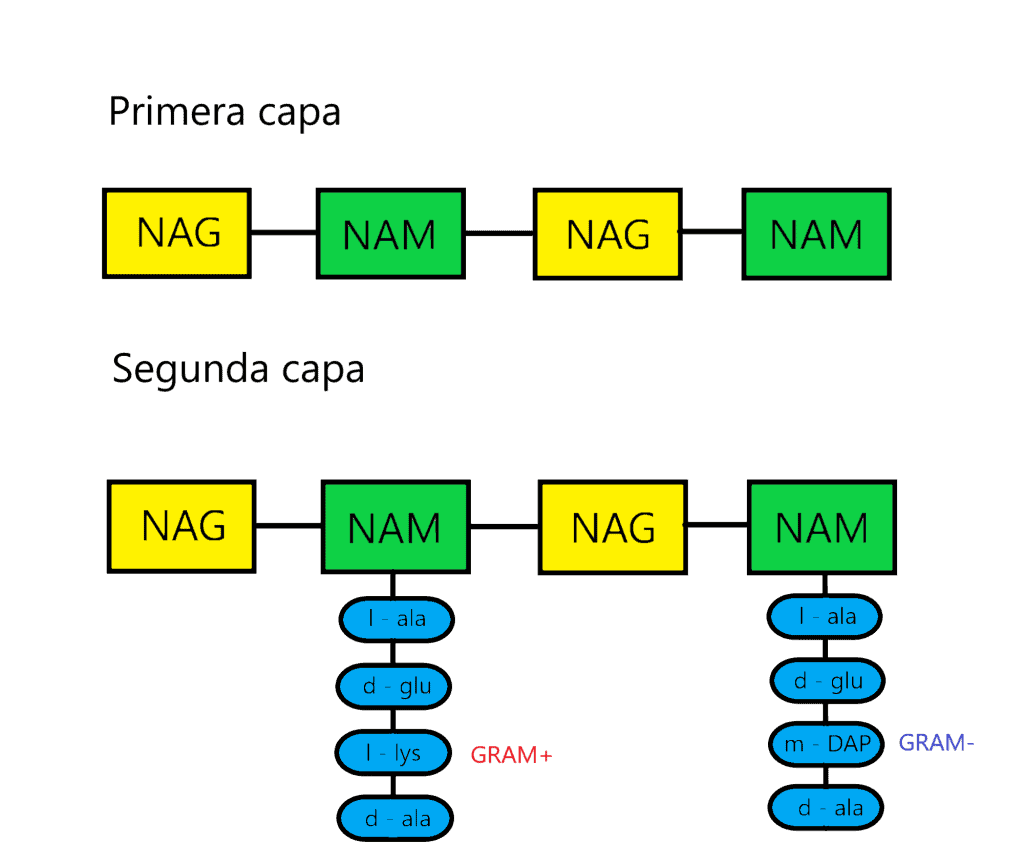
Como se puede ver, aquí aparecen proteínas formadas tanto de d-aminoácidos como de l-aminoácidos, de ahí una de sus particularidades (ya que las células usan solo l-aminoácidos para formar proteínas).
La tercera capa está formada por la unión de dos NAM vecinos. Para ello, la mayoria de veces se forma un enlace peptídico entre el cuarto aminoácido de un tetrapéptido (d-alanina) y el tercero de otro (L-lisina o m-DAP) mediante una reacción de transpeptidación. La composición de estos puentes peptídicos varía entre los diferentes grupos bacterianos; de hecho, los aminoácidos y la posición de este enlace se ha usado para clasificarlos (taxonomía). En bacterias GRAM- y algunas especies de Bacillus el enlace es directo, entre la D-alanina y el ácido diaminopimélico (m-DAP). En la mayoría de bacterias GRAM+ hay un puente formado por uno o más aminoácidos. Ejemplos:
- Staphylococcus aureus. Puente formado por 5 residuos de glicina.
- Micrococcus roseus. Puente formado por 3 L-alaninas y 1 L-treonina.
- Staphylococcus epidermidis. Puente formado por 3 glicinas y 2 L-serinas.
A veces el puente es desde el aminoácido D-alanina terminal hasta el α-carboxilo de ácido D-glutámico del otro tetrapéptido. Debido a que hay una conexión entre 2 grupos carboxilo, es necesario que el puente contenga diaminoácidos.
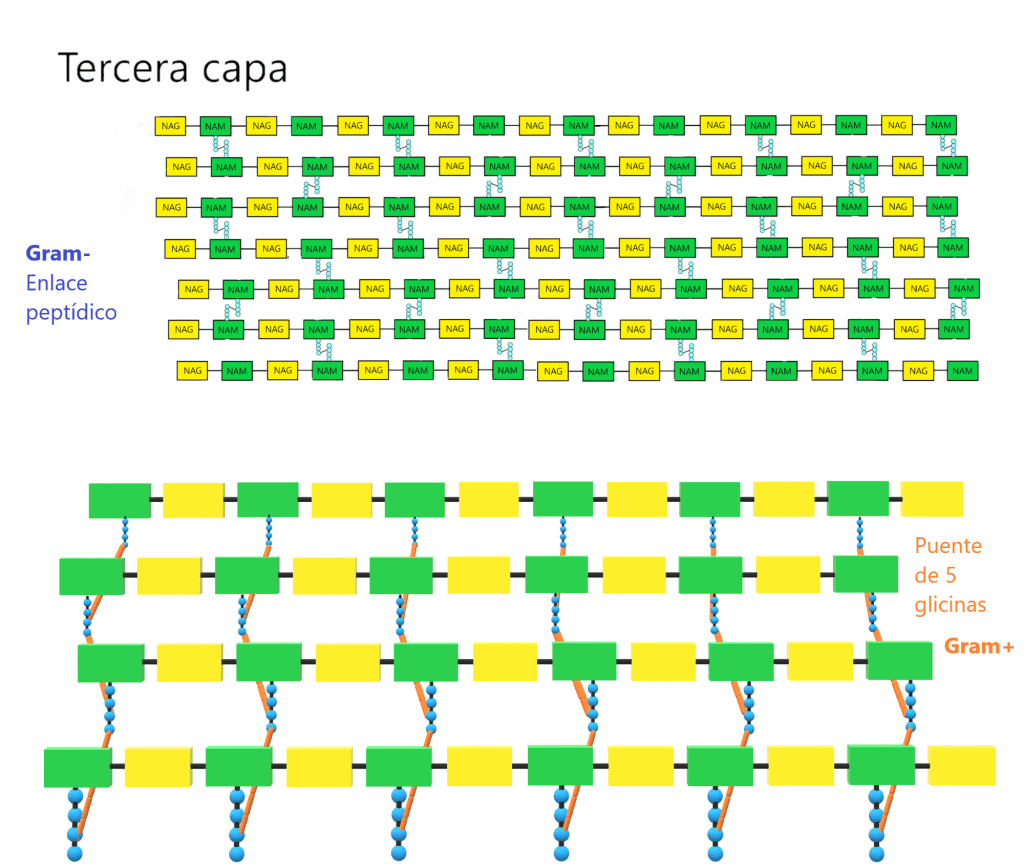
Estas tres capas forman la estructura tridimensional que da rigidez a la pared. Aunque pueden haber variaciones en la parte proteica del peptidoglicano, los enlaces entre NAG y NAM iguales para todas las especies bacterianas. No todos los tetrapéptidos unidos a NAM sufren la reacción de transpeptidación. De hecho, la pared tiene que tener algo de porosidad para permitir el paso de sustancias por la pared. Además, para que la célula pueda replicarse, necesita dividirse, expandirise, y es otra razón por la que la pared debe tener cierta flexibilidad. Ahora bien, cuantos más tetrapéptidos sufren la reacción de transpeptidación, más resistente será la pared celular.
Biosíntesis del peptidoglicano
La síntesis del nuevo peptidoglicano ocurre durante el proceso de crecimiento celular. Hay cuatro fases en este proceso. Primero, se forman los precursores del PG, que son derivados UDP de aminoazúcares formados en el citosol. Después, los aminoazúcares se transfieren a un transportador lipídico de membrana que los lleva a los aminoazúcares a través de la membrana celular. Más adelante, el PG se formará en la superficie externa de la membrana. Por último, ocurrirá la reacción de transpeptidación que forma puentes entre tetrapéptidos de NAM.
Reacciones en el citosol
Los azúcares NAG y NAM son los precursores del PG. Ambos se forman a partir de la fructosa-6-fosfato. Las reacciones se pueden ver en la imagen de abajo. Todo empieza cuando la glutamina da un grupo amino a la fructosa-6-fosfato, que la convierte en glucosamina-6-fosfato (1) Esta reacción esta mediada por la enzima fructosa-6-fosfato aminotransferasa. Más tarde, una transacetilasa (glucosamina fosfato transacetilasa) transfiere un grupo acetilo que proviene del acetil-CoA al grupo amino de la glucosamina-6-fosfato, y forma la N-acetilglucosamina-6-fosfato (2). La N-acetilglucosamina-6-fosfato sufrirá un proceso de isomerización, mediada por la N-acetilglucosamina fosfomutasa que la transformará en N-acetilglucosamina-1-fosfato (3). Este monofosfato ataca a UTP, y desplaza el pirofosfato, cambiando el compuesto a UDP-N-acetilglucosamina (UDP-GlcNAc); reacción en la que interviene la enzima UDP-N-acetilglucosamina fosforilasa (4). A partir de aquí, algunos de los UDP-GlcNAc se usan como precursores de la N-acetilglucosamina, mientras que otros se convierten en ácido UDP-N-acetilmurámico (UDP-MurNAc).
UDP-GlcNAc se covierte en UDP-MurNAc añadiendo un grupo lactilo (5). Durante está reacción, mediada por la enolpiruvato transferasa, el grupo hidroxilo C₃ desplaza un fosfato del carbono α del fosfoenolpiruvato, formando el UDP-N-acetilglucosamina-3-enolpiruvatoéter. Después, el derivado de enol se reduce a una porción de lactilo mediante el NADPH, en una reacción llevada a cabo por la enzima UDP-N-acetilglucosamincenol-piruvato reductasa (6). UDP-MurNAc se acaba convirtiendo en pentapéptido UDP-MurNAc mediante la adición secuenciada de (7):
- L-alanina
- D-glutamato
- L-R₃ (aminoácido de la tercera posición que puede variar en función de la bacteria)
- Dipéptido D-alanil-D-alanina
- ATP
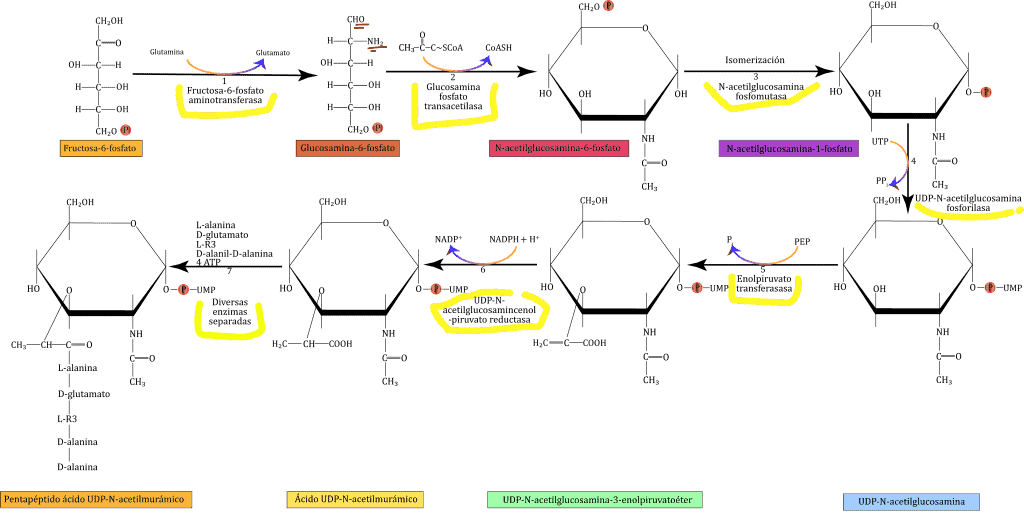
Cada reacción es catalizada por enzimas específicas y requiere ATP para activar el grupo carboxilo del aminoácido. El grupo carboxilo es un acil fosfato, que es atacado por el grupo amino que viene a unirse al aminoácido, desplazando el fosfato. Esta reacción produce ADP y un fosfato inorgánico. El dipéptido D-alanil-D-alanina se forma por la actuación de dos enzimas: la L-alanina-racemasa, que convierte L-alanina en D-alanina; y la D-alanil-D-alanil sintetasa dependiente de ATP, que forma D-alanil-D-alanina a partir de 2 D-alaninas. La quinta D-alanina se extraerá de esta estructura en el proceso de transpeptidación que veremos más adelante. Ambas enzimas, la racemasa y la sintetasa, son inhibidas por el antibiotico D-cicloserina.
Este pentapéptido UDP-MurNAc se transfiere al transportador lipídico en la membrana, y empiezan así los procesos en la membrana celular.
Reacciones en la membrana
El transportador lipídico que al que nos referimos es el bactoprenol (o undecaprenil-fosfato), un isoprenoide fosfato C55 hidrófobo. Además de transportar los precursores del PG, también mueve los precursores de otros polímeros, como el lipopolisacárido (LPS) o los ácidos teicoicos. Los nucleótidos azucarados se mueven por difusión a la superficie citoplasmática de la membrana, y allí el bactoprenol (lípido-P) ataca al pentapéptido UDP-MurNAc, liberando UMP (1). El producto es el pentapéptido lípido-PP-MurNac. GlcNAc se transfiere del UDP-GlcNAc a MurNAc en el transportador lipídico cuando el C4 hidroxilo en MurNAc ataca el carbono C1 en UDP-GlcNAc, liberando UDP (2). El compuesto resultante es el disacárido precursor del PG, pentapéptido lipido-PP-MurNAc-GlcNAc. Este compuesto se moverá al otro lado de la membrana (3). Si bien no se sabe exactamente como se mueve a través de la membrana, parece ser que es ayudado por proteínas aun por identificar.
Las proteínas fijadoras de penicilina (PBP), o autolisinas, estarán envueltas en los procesos de transglicosilación, transpeptidación y carboxipeptidación. En el lado externo de la membrana, este compuesto es transferido al glicano en formación y se sitúa en la parte final de la cadena. Esta reacción es una transglicosilación en la cual el C4 hidroxilo de GlcNAc en formación ataca el C1 de MurNAc del glicano, desplazando el bactoprenol de la cadena de glicano que se está formando (4,5). Esta reacción es catalizada por una enzima transglicosilasa ligada a la membrana (PBP-1a y PBP-1b).
No obstante, la cadena de glicano en formación sigue anclada a la membrana por el carrier lipídico en el sitio de la transglicosilasa. El lípido-PP formado por la cadena en formación se hidroliza por una pirofosfatasa ligada a la membrana, que forma lípido-P y libera un fosfato (6). Esta reacción es de suma importancia, ya que finaliza la reacción de transglicosilación, debido a que la hidrólisis del fosfodiester libera energía (el fosfato). Además, así se vuelve a formar el lípido-P (bactoprenol) que se puede reutilizar para la formación de PG u otros polímeros (7). Esta hidrólisis es inhibida por el antibiótico bacitracina.

El proceso de síntesis de peptidoglicano debe estar perfectamente coordinado. Los nuevos tetrapéptidos se deben unir al PG existente justo después de que las autolisinas actúen. Sino, se formaría una brecha en la integridad del PG en el punto de empalme, que podría desembocar en la lisis espontánea de la bacteria (autolisis).
Cross-linking. Transpeptidación
Para formar los puentes peptídicos entre los tetrapéptidos de NAM de cadenas adyacentes y así unir a los péptidos (cross-linking) hace falta energía. La transpeptidación es el proceso por el cual se obtiene energía necesaria para unir a los péptidos. En el peptidoglicano maduro, un grupo NH₂ del diaminoácido de la tercera posición (por ejemplo, el diamino-pimélico) ataca el carbonilo (C=O), desplazando el aminoácido D-alanina terminal (hidrolización). Este proceso está mediado por transpeptidasas (PBP-1a y PBP-1b). Los residuos D-alanina terminales que no participan en estas uniones también se eliminan, pero este proceso lo lleva a cabo la carboxipeptidasa D-alanina (PBP-4, PBP-5 y PBP-6). Diversos antibióticos, como la penicilina, inhiben esta reacción.
Azul: NAG
Naranja: NAM
Verde: enlaces β(1→4), entre el C1 de NAM y el C4 de NAG
Violeta: Enlace entre dos NAM de distintas líneas.
Los antibióticos y el peptidoglicano. ¿Qué ocurre si no se produce peptidoglicano?
Como ya hemos comentado, la pared celular tiene muchas funciones, y una de ellas es resistir la presión osmótica interna de la bacteria. El peptidoglicano es de suma importancia para que la pared celular tenga las propiedades que necesita la bacteria. De hecho, si se inhibe la biosíntesis del peptidoglicano o su degradación especifica durante el crecimiento celular esto acabará desembocando en la lisis de la célula (destrucción de la célula). Por ese motivo, usamos diversos antibióticos que atacan dichos procesos. Veamos varios antibióticos que se usan para el tratamiento antimicrobiano:
- Fosfomicina. Derivado del ácido fosfórico que inhibe la actuación de la enzima enolpiruvato transferasa, ya que es análogo del fosfoenolenilpiruvaoto (PEP). Es sintetizada por Streptomyces fradiae.
- D-cicloserina. Análogo de D-alanina que inhibe la conversión de L-alanina en D-alanina llevada a cabo por la enzima racemasa. Sintetizada por Streptomyces archidaceus.
- Bacitracina. Se une al bactoprenol fosforilado, e impide su desfosforilación. De esta forma se evita su reutilización para la formación de PG. Es sintetizado por Bacillus licheniformis y Bacillus subtilis. Se usa contra bacterias GRAM+.
- Vancomicina. Se une el dipéptido D-alanil-D-alanina (2 residuos de D-alanina) mediante puentes de hidrógeno. De esta forma se evita la reacción de transglicosilación que une el glicano en formación al peptidoglicano ya existente. Sintetizada por Streptomyces orientalis.
- Mureidomicinas. Se unen al bactoprenol ya que son análogos del pentapéptido UDP-MurNAc, evitando así su tranporte a la membrana plasmática. Son sintetizadas por Streptomyces flavidivirens.
- β-lactámicos. Bloquean la actividad transpeptidasa de las proteínas fijadoras de penicilina (PBP) relacionadas con las reacciones de transglicosilación, transpeptidación y carboxipeptidación. De esta forma, la formación de PG disminuye, lo que desemboca en la muerte de la bacteria, sea por no aguantar la presión osmótica o por enzimas autolíticas.
- Penicilinas. Sintentizadas por el hongo Penicillium. Clasificación:
- Penicilinas naturales. Penicilina G, Penicilina V. Se usan contra cocos GRAM+.
- Resistentes a penicilinasas. Oxalicina, meticilina, cloxacilina. Se usa contra GRAM+, destacando a Stafilococcus aureus productor de β-lactamasa.
- De amplio espectro. Ampicilina, amoxicilina, amoxicilina con ácido clavulánico. Se usa frente a cocos GRAM+ y algunas GRAM-.
- Anti-pseudomonas. Carbenicilina, piperacilina/tazobactam. Se usa contra Pseudomonas aeruginosa y bacterias GRAM- que aparecen en hospitales.
- Cefalosporinas. Sintetizadas por Cephalosporium. Tienen un espectro más amplio que las penicilinas. Hay 4 grupos:
- 1ª generación. Ejemplo: Cefalotina. Se usan especialmente contra GRAM+.
- 2ª generación. Ejemplo: Cefoxitina. Se usa frente a muchos organismos GRAM- y algunos GRAM+.
- 3ª generación. Ejemplo: Cefoperazona. Son más eficaces contra bacterias GRAM-.
- 4ª generación. Ejemplo: Cefepime. Espectro muy amplio.
- Penicilinas. Sintentizadas por el hongo Penicillium. Clasificación:
Diferencias entre GRAM positivas y GRAM negativas
El peptidoglicano, si bien es un compuesto común de las bacterias, tiene diferencias entre organismos GRAM+ y GRAM-, como los que veremos a continuación (en la tabla final se puede ver un resumen de estas).
En bacterias GRAM+, el peptidoglicano ocupa hasta el 90% de la pared celular. Pueden aparecer bacterias con solo una capa de peptidoglicano rodeando a la célula, pero la mayoría de bacterias cuenta con muchas láminas apiladas unas sobre otras. Eso sí, la capa se sitúa en el exterior de la membrana plasmática. En la tinción de Gram, dentro de las células se forma un complejo cristal violeta-yodo que NO puede extraerse. Y es debido a sus gruesa pared celular formada por varias capas de peptidoglicano. Al introducir alcohol, se deshidratan, lo que provoca el cierre de los poros de las paredes, así que el colorante no sale de la bacteria. Además, en bacterias GRAM+ aparecen los llamados ácidos teicoicos. Son polímeros de la pared que contienen unidades de glicerolfosfato o de ribitolfosfato. También pueden tener unidos otros azúcares y d-alanina. Los ácidos teicoicos se unen mediante enlace covalente a residuos de NAM. Pueden intervenir uniendo calcio (Ca2+) y magnesio (Mg2+) para su transporte. Tienen carga negativa, así que tienen su parte de responsabilidad de la carga negativa de la superficie celular.
En bacterias GRAM-, el peptidoglicano ocupa hasta el 10% de la pared celular. Está situada entre la membrana externa y la membrana interna de la célula. La mayor parte de la pared celular está formada por la membrana externa, una segunda bicapa lipídica que, aparte de fosfolípidos y proteínas, también contiene polisacáridos. A esta membrana se le llama lipopolisacárido (LPS). En la tinción de Gram, dentro de las células se forma un complejo cristal violeta-yodo que puede extraerse. Y es debido a que la membrana externa es rica en lípidos, además de que la capa de peptidoglicano es tan fina que no impide el paso del solvente, así que el colorante sale de la célula. Después del tratamiento con alcohol, estas bacterias reciben una tinción de contraste, la safranina, para diferenciarse de las bacterias GRAM+.
| Diferencias entre bacterias GRAM+ y GRAM- | ||
|---|---|---|
| Bacterias | GRAM+ | GRAM- |
| Tamaño de PG | Hasta 90% de la pared celular | Hasta el 10% de la pared celular |
| Localización del PG | Al exterior de la membrana plasmática | Entre la mebrana interna y la membrana externa |
| Tinción de GRAM | Complejo cristal violeta-yodo | Safranina |
| Color en la tinción de GRAM | Azul, violeta | Rojo, rosa, naranja |
| Tercer aminoácido del tetrapéptido | L-lisina normalmente; mucha variación de aminoácidos | m-DAP casi siempre; poca variación de aminoácidos |
| Transpeptidación (cross-linking) | Casi siempre puente de aminoácidos | Casi siempre enlace directo |
| Compuestos unidos a PG | Ácidos teicoicos | Lipopolisacárido (LPS) |
Pseudopeptidoglicano: estructura y función
¿Qué se entiende por pseudopeptidoglicano?
El pseudopeptidoglicano, también conocido como pseudomureína, es uno de los principales componentes de la pared celular de ciertas arqueas metanogénicas. Aunque su estructura química es diferente a la del peptidoglicano de las bacterias, ambos cumplen funciones similares en la protección y rigidez de la célula.
Estructura del pseudopeptidoglicano
A nivel estructural, el pseudopeptidoglicano está compuesto por dos azúcares: N-acetilglucosamina (NAG) y ácido N-acetiltalosaminurónico (NAT). Esta diferencia clave con el peptidoglicano bacteriano, que contiene ácido N-acetilmurámico (NAM) en lugar de NAT, se refleja también en los enlaces que forman la cadena. En el pseudopeptidoglicano, los azúcares están unidos por enlaces β-1,3-glicosídicos, a diferencia de los β-1,4-glicosídicos presentes en el peptidoglicano.
Esta estructura única hace que el pseudopeptidoglicano sea resistente a la lisozima, una enzima presente en las secreciones humanas como saliva y lágrimas, que descompone el peptidoglicano bacteriano al romper los enlaces β-1,4. Al no poder actuar sobre los enlaces β-1,3 del pseudopeptidoglicano, la lisozima se vuelve ineficaz frente a las arqueas que poseen este polímero en sus paredes celulares.
Diferencias con el peptidoglicano
Existen varias diferencias importantes entre el peptidoglicano bacteriano y el pseudopeptidoglicano de las arqueas:
- Composición química: Mientras que el peptidoglicano contiene N-acetilglucosamina y ácido N-acetilmurámico, el pseudopeptidoglicano contiene N-acetilglucosamina y ácido N-acetiltalosaminurónico.
- Enlaces glicosídicos: Los enlaces entre los azúcares en el peptidoglicano son de tipo β-1,4, mientras que en el pseudopeptidoglicano son de tipo β-1,3, lo que confiere una mayor resistencia a ciertas enzimas degradativas.
- Distribución: El peptidoglicano se encuentra en la mayoría de las bacterias, mientras que el pseudopeptidoglicano es exclusivo de algunas arqueas metanogénicas.
Función del pseudopeptidoglicano
Al igual que el peptidoglicano en las bacterias, el pseudopeptidoglicano en las arqueas tiene la función de proporcionar rigidez estructural y protección frente a condiciones externas adversas. Actúa como una barrera, ayudando a las células a mantener su forma y protegiéndolas de factores ambientales perjudiciales.
Además, debido a su composición única, es resistente a ciertos antibióticos que atacan la pared celular bacteriana, como la penicilina, que resulta ineficaz contra el pseudopeptidoglicano debido a las diferencias en las enzimas implicadas en la reticulación de los aminoazúcares.
Evolución del pseudopeptidoglicano
El pseudopeptidoglicano ofrece una ventana a las estrategias evolutivas de las arqueas frente a las bacterias. Su resistencia a enzimas bacterianas, como la lisozima, y su insensibilidad a ciertos antibióticos demuestran cómo las arqueas han desarrollado adaptaciones únicas para sobrevivir en ambientes extremos.
Estas características podrían haber sido moldeadas por las presiones evolutivas en entornos inhóspitos, como los océanos profundos o los hábitats metanogénicos, donde las arqueas prosperan.
Referencias
Calvo. J, Martínez-Martínez. L, Mecanismos de acción de los antimicrobianos. (2009) Enfermedades Infecciosas y Microbiología Clínica, Volume 27, Issue 1, Pages 44-52, ISSN 0213-005X. DOI: 10.1016/j.eimc.2008.11.001.
Mensa. J, Gatel. J. M, García-Sanchez. J. E, Letang. E, López-Suñe. E, Marco. F. (2018) Guia de terapeútica antimicrobiana 2018, Editorial: Antares, Nº de edición: 28ª, ISBN-13: 9788488825247
Mechthild Pohlschroder, Friedhelm Pfeiffer, Stefan Schulze, Mohd Farid Abdul Halim, Archaeal cell surface biogenesis, FEMS Microbiology Reviews, Volume 42, Issue 5, September 2018, Pages 694–717, https://doi.org/10.1093/femsre/fuy027
Michael T. Madigan. (2015) Brock: biología de los microorganismos. Edición 14. Pearson Educación. ISBN: 8490352798, 9788490352793
Vollmer, W., & Höltje, J. V. (2000). A simple screen for murein transglycosylase inhibitors. Antimicrobial agents and chemotherapy, 44(5), 1181–1185. https://doi.org/10.1128/aac.44.5.1181-1185.2000
Vollmer W, Blanot D, de Pedro MA. (2008) Peptidoglycan structure and architecture. FEMS Microbiol Rev. 2008;32(2):149‐167. doi:10.1111/j.1574-6976.2007.00094.x
White, D., Drummond, J., & Fuqua, C. (2012). The physiology and biochemistry of prokaryotes. New York: Oxford University Press.
