Fototrofía. Fotosíntesis Oxigénica y Anoxigénica
La fotosíntesis es un proceso vital no solo para las plantas, sino también para diversos microorganismos que juegan un papel fundamental en la producción de oxígeno y la conversión de energía solar en energía química. Aproximadamente más de la mitad de la fotosíntesis en el planeta es realizada por microorganismos fotótrofos, lo que resalta su relevancia ecológica y su papel en el mantenimiento del equilibrio atmosférico y energético de la Tierra.
Este proceso se divide en fases que involucran la absorción de luz y la transformación de compuestos inorgánicos en orgánicos, siendo clave para la fijación de dióxido de carbono. Las diferencias entre la fotosíntesis oxigénica y anoxigénica, así como los pigmentos fotosintéticos y estructuras celulares asociadas, destacan la diversidad de mecanismos que permiten la vida bajo diversas condiciones ambientales.
Índice de contenidos
Fotosíntesis
Dentro del metabolismo microbiano nos vamos a centrar en el proceso de fotosíntesis. Más de la mitad de la fotosíntesis de todo el planeta la realizan los microorganismos fotótrofos.
La fotosíntesis, como definición general, es un mecanismo que permite capturar la energía luminosa y convertirla en energía química (ATP). Esto va a permitir la reducción (fijación) del CO2 hasta compuestos orgánicos. Se puede diferenciar la fotosíntesis en dos fases:
- Fase luminosa. Requiere luz. Se obtiene ATP y poder reductor en forma de NADPH, que van a ser utilizados en la fase oscura.
- Fase oscura. No necesita luz, con tal de que exista ATP y NADPH para fijar/ reducir el CO2 a compuestos orgánicos.
La inmensa mayoría de los fotótrofos son fotoautótrofos.
Hay que diferenciar dos tipos de fotosíntesis:
Fotosíntesis oxigénica
Se genera oxígeno. Es la típica de plantas, algas, y un grupo importante de bacterias: las cianobacterias.
En este tipo de fotosíntesis la fuente de poder reductor en el agua: mediante la fotólisis del agua se desprende un producto de desecho para las plantas, el O2. Tanto para obtener ATP como NADPH hace falta la presencia de luz.
También se la denomina fotosíntesis vegetal.
Fotosíntesis anoxigénica
No produce oxígeno. Se da en bacterias rojas, verdes y heliobacterias. No se emplea el agua como fuente de poder reductor; se usan otros compuestos orgánicos o inorgánicos distintos del agua por lo que no se produce O2. Produce las formas oxidadas del NAD y el FAD. Requiere ausencia total de O2.
La obtención de ATP gracias a la luz se denomina fotofosforilación. También se la denomina fotosíntesis bacteriana.
Pigmentos fotosintéticos
Para llevar a cabo la fotosíntesis se requieren unos pigmentos especiales para captar esa energía luminosa. Cuanto menor en la longitud de onda, mayor es la energía de la radiación absorbida. En la fotosíntesis oxigénica la luz es captada por la clorofila; en la fotosíntesis anoxigénica es captada por la bacterioclorofila (Bclorofila).
Las clorofilas transmiten luz verde porque absorben principalmente en la zona roja del espectro.
Las bacterioclorofilas tienen un espectro de absorción con máximos a longitudes de onda más largas, más en la zona infrarroja. Este desplazamiento de los máximos de absorción adapta mejor a estas bacterias a sus nichos ecológicos.
Ambas son similares en estructura. Constan de un núcleo porfirínico central (son porfirinas) con el anillo tetrapirrólico central que contienen en el interior un ion metálico quelado. Además, tienen una cadena lateral de fitilo (20C con grupos metilo y grupos hidrófobos) o de geranil-geranilo (20C).
La localización de los pigmentos depende del tipo de fotosíntesis:
- Las cianobacterias presentan unas membranas multilaminares, también denominadas tilacoides, no porque sean iguales sino por analogía de función. Esas membranas suelen disponerse de manera concéntrica en la periferia del citoplasma.
- En bacterias rojas (o purpuras o purpureas) los pigmentos están en invaginaciones de la membrana plasmática, que pueden estar formando laminas planas (denominadas lamelas) o pueden formar tubos de sección circular (denominadas vesículas). Ambos casos son continuos con la membrana plasmática.
- En bacterias verdes parte de los pigmentos están en la membrana plasmática, pero también se pueden encontrar en los clorosomas (vesículas especiales limitadas por una membrana proteica que están adheridas a la superficie de la membrana plasmática por una membrana basal). Estos clorosomas son muy eficientes en la captación de la luz, por lo que no necesitan mucha intensidad luminosa para llevar a cabo la fotosíntesis. De hecho, las bacterias verdes se encuentran a mayor profundidad que el resto de fotótrofos.
- En las heliobacterias la misma membrana plasmática dispone de los pigmentos.
Pigmentos accesorios de antena
Además de los pigmentos principales (clorofilas y Bclorofilas), hay otros que también absorben la energía luminosa: pigmentos accesorios de antena. Hay de dos tipos: carotenoides y ficobiliproteinas.
Carotenoides
Son largas cadenas isoprenoides (con dobles enlaces conjugados) que suelen presentar, aunque no siempre, anillos de ciclohexeno sustituidos. Suelen tener color purpura, rojo o amarillo y absorben en la zona azul del espectro (desde 450 a 500nm). Son liposolubles. Existe aproximadamente el mismo número de moléculas de carotenoides que se clorofila/Bclorofila. Capturan la energía luminosa y la transmiten a la clorofila/Bclorofila, pero no participan activamente en las reacciones de fotoactivación. Podemos diferenciar dos tipos:
- Carotenos. Son carotenoides hidrocarbonados. Ejemplo: el beta-caroteno.
- Xantofilas. Son carotenoides oxigenados.
Hay diferencias entre los carotenoides que presentan los organismos fotótrofos.
Ficobiliproteínas
Son realmente cromoproteínas (un tipo de heteroproteínas), solubles en agua y que contienen tetrapirroles lineales denominados ficobilinas.
Se encuentran formando agregados de elevado peso molecular denominados ficobilisomas, unidos a las membranas fotosintéticas. El contenido celular de los ficobilisomas aumenta cuando desciende la intensidad de luz, es como un mecanismo de compensación.
No están presentes en plantas, ni en la mayoría de las bacterias. Están en algas rojas (eucariotas), y en cianobacterias. Hay dos ficobiliproteínas principales:
- Ficoeritrina. Pigmento rojo principal de las algas rojas, con una absorción máxima de entre 550-560nm.
- Ficocianina. Pigmento azul característico de las cianobacterias, con una absorción máxima de entre 620-640nm. La ficocianina está compuesta por una ficobilina y una proteína. La ficobilina de esta ficocianina es la ficocianobilina.
Funciones de los pigmentos accesorios de antena
- Amplían el rango de λ que puede absorber (absorben en el rango de 470-630nm); hacen más eficaz la fotosíntesis en un espectro más amplio de λ, ya que transfieren la energía a la clorofila/ Bclorofila.
- Al tratarse de un gran número de moléculas aumentan la velocidad de captación de la luz.
- Principalmente los carotenoides son agentes fotoprotectores de reacciones de fotooxidación: protegen a los microorganismos de la luz solar intensa que podría dañar al aparato fotosintético. Actúan como escudo para clorofila/ Bclorofila fotosensible.
Es una ventaja para los microorganismos que viven en presencia de luz.
Estructura general del aparato fotosintético
Es el aparato fotoquímico responsable de la fotosíntesis. Es la unidad estructural y funcional encargada de captar la energía luminosa y convertirla en energía química. Podemos diferenciar 3 elementos:
- Complejo antena. Está constituido por 200-300 moléculas de clorofila/Bclorofila + pigmentos accesorios. Son los responsables de absorber la radiación de una determinada longitud de onda y canalizar esa energía hasta el centro de reacción. La transfieren en paquetes denominados excitones, por un mecanismo de resonancia inducida: las moléculas de pigmento actúan a modo de embudo, pero ellas no se fotoactivan, solo la transfieren.
- Centro de reacción. En donde tiene lugar el proceso fotoquímico. En él se encuentra la clorofila/ Bclorofila del par especial: esas son las que se fotoactivan en presencia de luz y entonces pasan de un estado basal a un estado excitado en el cual P va a ser un potente reductor, que va a pasar los electrones (e-) a I (P se reduce e I se oxida). I = feofitina/Bfeofitina (como una clorofila sin magnesio).
- Cadena de transporte electrónico. A continuación, este electrón va a pasar a un componente: el primer aceptor estable, que recibe el electrón del aceptor primario (I) y lo cede a una cadena de transporte de electrones.
Este primer aceptor estable puede ser o una quinona o una Fe-S proteína. El par oxidado ha quedaso oxidado, y debe volver a su estado basal, para lo que necesita un electrón que puede provenir de la CTE o de un dador externo.
Todo este proceso realmente le va a permitir sintetizar ATP, ya que ese flujo de electrones conduce a la creación de un gradiente de protones (fuerza protón-motriz) lo que va a ser aprovechado por una ATPasa de la membrana. Como la síntesis de ATP se realiza gracias a la acción de la luz se denomina fotofosforilación.
Fotosíntesis bacteriana o anoxigénica. Componentes de aparato fotosintético
Solo tiene un fotosistema (PS) y emplea Bclorofila. No utiliza H2O, por lo que no desprende O2. Se realiza exclusivamente en condiciones anóxicas: no solo no generan oxígeno, sino que no lo toleran. La síntesis de ATP es por fosforilación cíclica.
La Bclorofila se oxida cuando llegan los fotones de luz roja o infrarroja. Se carga positivamente y los electrones pasan a la CTE. Esto les permite sintetizar ATP, ya que aprovechan la fuerza protón-motriz gracias a las ATPasas de membrana. Como este proceso se desencadena por la luz, se denomina fotofosforilación.
Los electrones viajan de los potenciales más electronegativos a los más electropositivos.
Bacterias rojas
El centro de reacción se denomina P870. Contiene Bclorofila: 4 moléculas, dos de las cuales constituyen el par especial y las otras dos el de bacteriofeofitina A (I).
Con la llegada de la luz, el P870 pasa de un estado basal a un estado excitado (P870*). En este estado, actúa como un potente reductor y le cede sus electrones a la bacteriofeofitina A (que se reduce). A continuación, se lo cede a varias moléculas de quinona, y al final van a un pool de quinonas que hay en la membrana. Desde la quinona van pasando los electrones a transportadores de la cadena. Al final ese electrón vuelve a P870 que había quedado oxidado y debe volver a su estado basal para volver a absorber luz y repetir el proceso.
Es muy importante la disposición de estos elementos en la membrana. Gracias al gradiente de protones que se va produciendo se puede sintetizar el ATP. La ATPasa aprovecha ese gradiente, lo va reduciendo y a su vez va produciendo ATP. Producen una fotofosforilación cíclica.
Bacterias verdes del azufre y heliobacterias
El ATP también se obtiene por fotofosforilación cíclica. Comparten mecanismos básicos, aunque se diferencian en los pigmentos. Son más parecidas entre sí y diferentes a las rojas.
Comparten tres importantes características:
- Tienen clorofila A, o hidroxiclorofila A (en esencia son lo mismo) como aceptor primario.
- Tienen una proteína Fe-S como aceptor estable de electrones (Z) con un potencial de -0’6V. Esto en las bacterias rojas era el pool de quinonas, con un potencial de -0’15V.
- Tienen ferredoxina con un potencial de -0’39V (también está en cianobacterias). También la vamos a ver en los fotótrofos oxigénicos.
Las bacterias verdes no del azufre tienen un centro de reacción y un mecanismo de fotosíntesis más parecido al de las bacterias rojas que las que si son del azufre. Por ejemplo, Z se parece en su potencial al de las rojas, más que al de las verdes. Son muy pocas: básicamente se refiere al género Chloroflexus.
Obtención del poder reductor
En ambos casos se produce fotofosforilación cíclica. Necesitan fijar CO2, para lo que necesitan poder reductor (NADH/ NADPH).
Para obtenerlo, hay que tener en cuenta los potenciales redox para saber por qué en algunos casos estas bacterias realizan un transporte inverso de electrones y en otros no. Los fotótrofos anoxigénicos no usan el agua como fuente de poder reductor.
Se conocen al menos 3 modos de transferencia de electrones desde los donadores externos hasta el NAD/NADP:
Transferencia directa
Transferencia directa desde un compuesto altamente reducido. Si el compuesto tiene un potencial más bajo, puede reducir el NAD/NADP.
Transporte inverso de electrones
En bacterias rojas, cuando crecen utilizando donadores de electrones con potenciales más altos que el del NAD/NADP necesitan realizar transporte inverso de electrones.
Los electrones de ese depósito de quinonas tienen que moverse hacia atrás en contra del gradiente del potencial electroquímico para reducir finalmente el NAD/NADP. Los electrones se mueven en una dirección termodinámicamente desfavorable: desde el pool de quinonas al NADH. Tienen que gastar energía para moverse.
Donadores externos
En bacterias verdes del azufre y en heliobacterias presentan un transporte de electrones que permite reducir el NADP aunque empleen donadores externos con potenciales más altos que los del par NADP/NADPH. En ambos casos la CTE se produce entre la Bclorofila del centro de reacción al primer transportador de electrones, la proteína Fe-S, que lo suficientemente electronegativa como para reducir a la ferredoxina y es, por tanto, más reductora que la quinona de bacterias rojas. La ferredoxina puede reducir directamente al NADP a NADPH sin que haga falta transporte inverso de electrones.
Todo depende del potencial ε’O:
Si ε’O (Z) < ε’O (NADP/NADPH) hay transporte normal de electrones.
Si ε’O (Z) > ε’O (NADP/NADPH) hay transporte inverso de electrones.
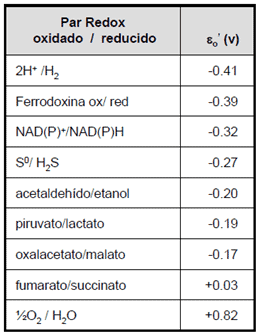
Cuando los electrones salen del ciclo para reducir al NAD/NADP/FAD, tienen que ser repuestos para que la fotofosforilación pueda continuar. Esos electrones son repuestos por los donadores externos, que cederían sus electrones a un componente de la cadena con un potencial más alto que el suyo.
El fotosistema es el que aporta la fuerza protón-motriz para que se produzca el transporte inverso de electrones, que es necesario por el hecho de usar donadores con potenciales más altos que el del par NAD/NADH. La ferredoxina también es importante en las verdes del azufre para la fijación del CO2, por el ciclo de TCA inverso.
En las bacterias que no son del azufre, Z presenta un potencial que impide la reducción directa del NADP: necesita un transporte inverso de electrones como en bacterias rojas.
En general, los fotótrofos anoxigénicos realizan la fotosíntesis en lugares con ausencia de oxígeno. Las que se denominan del azufre (tanto rojas como verdes) son fotoautótrofas obligadas (solo fotosíntesis en ausencia de oxígeno y tienen que fijar CO2). Las que se denominan no del azufre son fotoheterótrofas, pero son muy versátiles (pueden fotosintetizar, respirar, fermentar, vivir en ausencia de luz, etc; pero cuando fotosintetizan debe de ser en ausencia de oxígeno, que impide la síntesis de la Bclorofila).
Fotosíntesis vegetal u oxigénica
Usa clorofila A y H2O como donador de electrones (fuente de poder reductor). Actúan dos fotosistemas coordinadamente: P680 (fotosistema II, absorbe ene l rojo) y P700 (fotosistema I, absorbe en el infrarrojo).
Esta fotosíntesis se denomina vegetal, aunque también está presente en cianobacterias.
Al llegar luz a la antena del fotosistema II (P680), la energía se transfiere a la clorofila A del par especial, que se fotoactiva (desciende su potencial redox), se excita y se convierte en un reductor potente, que cede electrones a un aceptor: la feofitina. Aquí queda el electrón. Llegan 2 fotones.
Al ceder el electrón, la clorofila de P680 queda oxidada, hay que volver a reducirla: por los electrones procedentes de la fotolisis del agua (que libera H2 + O2 + e-). El electrón que pasa a la feofitina es repuesto por el que cede el agua. Los electrones van al P680, y parte de los H+ permanecen en el espacio tilacoidal (gradiente de H+).
La feofitina cede los electrones a un pool de quinonas que a su vez los cede a una CTE (formada por una plastoquinona, CitB6, Fe-S y CitF) que a su vez los cede a una plastocianina (que contiene cloro) que cede los electrones a P700 (fotosistema I). Para que P700 acepte el electrón debe de estar oxidado. Para ello previamente la antena de P700 ha tenido que captar luz, que se excita. P700 se convierte en un potente reductor. De ahí los cede a una feofitina A o un centro Fe-S, a otro centro Fe-S y finalmente a una ferredoxina.
Una vez que los electrones han llegado a la ferredoxina, pueden seguir dos vías:
Vía no cíclica
En la NO cíclica llegarían al final al NADP (reducen el NADP a NADPH). La ferredoxina quedaría oxidada a la espera de nuevos electrones. Intervienen los dos fotosistemas: se requiere la participación del PSII para reponer electrones. Se desprende oxigeno: por la fotólisis del agua que repone los electrones que pierde P680.
Además, se sintetiza ATP: las ATPasas de la membrana tilacoidal van a aprovechar la fuerza protón-motriz. A esta síntesis de ATP se denomina fotofosforilación no cíclica. Se desprende O2 a partir de la fotólisis del agua: entonces parte de los H + se destinan a reducir el NADP y parte a mantener el gradiente de protones del espacio tilacoidal.
Aquí los electrones no vuelven a P700 (por eso esta vía NO es cíclica).
En definitiva, el agua se necesita en última instancia para reducir el P700, pero como tiene un potencial tan alto que directamente no puede reducir a P700, pero lo que si puede hacer es reducir a la clorofila A de P680.
Vía cíclica
Cuando las células tienen suficiente NADPH, entonces vuelven a P700 en lugar de ir al NADP. Lo hacen a través un citocromo B (CitB563). En esta vía no se va a formar NADPH. Se sintetiza ATP en el mismo sitio que en la vía cíclica, pero en este caso es una fotofosforilación NO cíclica. Solo funciona el P700, por lo que no se va a desprender oxígeno.
Lo normal es que los dos fotosistemas funcionen juntos; sin embargo, en algunos organismos como algas y cianobacterias en algunos casos, pueden realizar fotosíntesis anoxigénica: usan solo el P700 y obtienen el ATP por fotofosforilación no cíclica.
En este caso necesitan un donador externo de electrones diferente del agua. En el caso de estas cianobacterias, emplean compuestos reducidos de azufre. Las algas suelen utilizar el hidrogeno. Esto lo pueden hacer en condiciones anoxigénicas, y deben tener ese donador de electrones externo. El donador dona los electrones al compuesto que lo puedan ceder mirando el potencial redox.
La forma de fijación del CO2 más extendida es el ciclo de Calvin. Aquí hacen falta el ATP y el NADH que se han producido.
Fotoautotrofía: ciclo de Calvin
Es la ruta más extendida para fijar el CO2. Requiere NADPH y ATP. Es la más habitual, pero no es la única. Se utilizan dos enzimas exclusivos de este ciclo: la rubisco y la fosforibulosa quinasa. El resto del ciclo lo catalizan varias enzimas que están presentes en numerosos organismos, tanto autótrofos como heterótrofos.
Vamos a considerar las reacciones del ciclo de Calvin basándonos en la incorporación de 6CO2 para calcular el balance de la síntesis de una molécula de hexosa.
Vamos a diferenciar tres fases:
Fase de fijación
El primer paso es la reacción catalizada por la rubisco (está presente en los fotótrofos oxigénicos, en las bacterias rojas, y en las bacterias quimiolitótrofas e incluso algunas arqueas hipertermófilas). Si presentan rubisco es lo mismo que decir que presentan este ciclo de Calvin.
En procariotas autótrofos estrictos fijan el CO2 en forma de carboxisomas (mecanismo para aumentar la concentración de la rubisco en la célula sin que afecten a la presión osmótica, aumentando así mucho la velocidad de fijación del CO2).
La rubisco cataliza la reacción de formación del ácido 3-fosfoglicerato a partir de ribulosa-1,5-bisfosfato. Luego ese 3-fosfoglicerato se transforma en 1,3-bisfosfoglicerato.
Fosforilación y reducción
El 1,3-BPG pasa a gliceraldehído-3-fosfato. Como es una reducción se va a producir un NADH. Ahora tenemos 12 moléculas de gliceraldehído-3-fosfato, de las cuales salen dos para formar glucosa por el camino inverso de los primeros pasos de la glucolisis; el resto (10) se quedan en el ciclo para regenerar el aceptor de CO2 (la ribulosa-1,5-bifosfato).
Regeneración del aceptor de CO2
Aquí aparece la ribulosa-1,5-bisfosfato. Hace falta 6ATP, que con los 12 anteriores son 18 en total.
6CO2 + 12 NADPH + 18 ATP → C6H12O6 (una molécula de hexosa) + 12 NADP + 18ADP
Cuando hay bastante ATP y NADH, las hexosas se puede formar polímeros de reserva que posteriormente podrán ser utilizados cuando sea necesario generar o construir el nuevo material general.
Ciclo del TCA inverso
Este ciclo de Calvin no es el único ciclo que permite fijar CO2: las bacterias verdes del azufre usan el ciclo del TCA inverso (ciclo de Krebs inverso). En lugar de salir el CO2, entra.
Estas bacterias verdes del azufre presentan dos enzimas unidas a ferredoxina: la ferredoxina es necesaria para las reacciones de carboxilación (las contrarias a la descarboxilación en el ciclo normal). El resto de reacciones están catalizadas por enzimas que trabajan invirtiendo la dirección normal del TCA.
Hay una excepción: la citrato liasa hace lo contrario que la citrato sintasa (de citrato a oxalacetato + Acetil-CoA).
Este ciclo también se ha encontrado en microorganismos como Sulfolobus y Thermophillus (arqueas) y Aquifex (bacteria).
Vía del hidroxipropionato
Hay otro ciclo particular: la vía del hidroxipropionato, que la usan las bacterias verdes NO del azufre. Hasta ahora esta ruta solo se ha podido confirmar en Chloroflexus: si consideramos que es la rama de los fotótrofos anoxigénicos más primitiva del dominio bacteria, por lo que se puede considerar que es la primera vía de fijación de CO2 en los fotótrofos.
Hay un intermediario que es el hidroxipropionato. Se fija CO2 en dos puntos.
Ni siquiera el ciclo de Calvin es universal entre los autótrofos. Esto es una prueba de la gran diversidad que hay entre los microorganismos.
