Quimiolitotrofía
Dentro del metabolismo microbiano aparece la quimiolitotrofía. Implica el uso de compuestos inorgánicos como fuente de energía (ATP) y donador de electrones (fuente de poder reductor). Obtienen el ATP por fosforilación oxidativa (PO), mediante una cadena de transporte electrónico (CTE). El donador de electrones es inorgánico y el aceptor terminal de electrones suele ser el oxígeno.
Analizando esta palabra se puede hallar su definición. Quimio- (del francés "chimio") hace referencia a química, lito- (del griego antiguo "lithos") hace referencia a rocas o piedras, y trofía (del griego antiguo "trophia") indica nutrición; de hecho, proviene del griego trophos, que significa alimento. Podemos deducir que los organismos que desarrollan la quimiolitotrofía se alimentan de piedras, o, en otras palabras, de compuestos inorgánicos.

La molécula transportadora de electrones es el NADH, que constituye el poder reductor. Éste se puede obtener directamente a partir del compuesto inorgánico que se oxida, cuando el par redox sea más bajo que el del NAD+/NADH. Lo habitual es que se requiera transporte inverso de electrones, con consumo de ATP.
En general, la autotrofía implica un requerimiento elevado de ATP. Muchos son autótrofos, usan como fuente de carbono el CO2, por el Ciclo de Calvin, que requiere tanto ATP como poder reductor. En general, la oxidación de compuestos inorgánicos libera muchísima menos energía que la oxidación de compuestos orgánicos, por lo que deben oxidar grandes cantidades de materia inorgánica para crecer. Por ello, se suelen desarrollar lentamente (poseen tiempos de generación muy elevados).
Hay diferentes grupos dependiendo de la fuente de carbono y de poder reductor; la gran mayoría se ubican dentro de las proteobacterias quimiolitótrofas.
Índice de contenidos
Oxidación del hidrógeno
Es una oxidación aeróbica (en este apartado no se va a tratar la oxidación anaerobia del oxígeno). Los oxidantes del H2 tienen una enzima denominada hidrogenasa que descompone el hidrógeno en dos protones y dos electrones. Los electrones pueden ir a una quinona o al NAD+, que irán a la cadena de transporte para producir ATP por medio de una fosforilación oxidativa.
Hay dos tipos de hidrogenasa: una hidrogenasa particulada ligada a la membrana y una hidrogenasa soluble (citoplasmática). La mayoría poseen una hidrogenasa particulada: los átomos de hidrógeno se transfieren a una quinona, y, a través de una serie de transportadores, llegan al aceptor final, el O2. En esta cadena de transporte electrónico se produce ATP. Aunque el potencial del par hidrógeno es más negativo que el del NADH no lo reducen directamente, sino a través de una quinona. Obtienen el ATP a través de transporte inverso de electrones.
Cuando poseen las dos, particulada y soluble, la particulada se especializa en la obtención de energía y la soluble en la obtención el poder reductor, ambos necesarios para la fijación del CO2.
La bacteria más característica de este grupo es Hydrogenobacter.
Oxidación del monóxido de carbono (CO)
Algunas especies además son capaces de crecer empleando el CO como única fuente de C y energía. A estas bacterias se les denomina carboxidobacterias. Oxidan el monóxido a dióxido y los electrones liberados son cedidos a la cadena de transporte obteniendo ATP por fosforilación oxidativa. El poder reductor lo obtienen por transporte inverso de electrones. El enzima clave es la deshidrogenasa de CO, que contiene molibdeno.
Oxidación de compuestos reducidos de azufre
Consiste en el uso de compuestos reducidos del azufre (sulfuros, azufre o tiosulfato), dependiendo del tipo de microorganismos, como fuente de energía y poder reductor. Lo presentan tanto bacterias como arqueas. El producto final de la oxidación son sulfatos y en ocasiones estos pueden convertirse en ácido sulfúrico, por lo que muchos son acidófilos.
El número total de electrones de sulfuro hasta sulfato es de 8.
- Partiendo de sulfuro, éste se oxida a sulfito y éste a sulfato, mediante la sulfuro oxidasa y la sulfito oxidasa respectivamente (en todos los microorganismos). También el sulfuro puede reaccionar con AMP dando adenosina fosfosulfato. Puede reaccionar este APS con fosfato liberándose sulfato y ADP. La enzima es la APS-reductasa. En este proceso obtienen ATP por fosforilación a nivel de sustrato, pues el ADP por la adenilato quinasa da lugar al ATP. En algunos tiene lugar la oxidación directa de los sulfuros a sulfatos (sistema Sox).
- Partiendo de tiosulfato, se descompone en sulfito y en azufre insoluble. Por tanto, usando tiosulfato se produce azufre, cosa que no ocurre con el uso de sulfuros. Cuando queda poco o nada de tiosulfato, el azufre también se oxida.
Tanto el sulfuro como el azufre pueden reaccionar con grupos sulfhidrilos celulares, como los del glutatión, dando complejos polisulfuro-sulfhidrilo. En todos los casos los electrones van a la cadena de transporte y se genera un gradiente protónico para la síntesis de ATP. Cuanto más corta sea la cadena, menos energía se obtiene. Se reduce el pH del medio, incluso por debajo de 1. Las bacterias son acidófilas estrictas.
El aceptor final suele ser el oxígeno, pero no todas son aerobias estrictas; hay algunas anaerobias facultativas donde el aceptor final en algunos casos es el nitrato. Esto ocurre en Thiobacillus denitrificans. El poder reductor se obtiene por flujo inverso de electrones, con consumo de energía. Lo normal es que sean autótrofas, pero no todas son estrictas; algunas son facultativas que usan compuestos orgánicos como fuente de carbono.
Oxidación de compuestos reducidos de hierro
El hierro tiene un potencial redox muy elevado. La oxidación proporciona poca energía por lo que se necesita oxidar grandes cantidades de hierro. Se forma el anión férrico (Fe3+), que en agua forma precipitados de hidróxido férrico insoluble. La mayoría son acidófilas estrictas, en parte porque a pH neutro en ambientes con oxígeno el ión ferroso (Fe2+) se oxida de forma espontánea y no biológica a Fe3+, por lo que no se acumula a grandes cantidades. Sólo es estable a pH neutro en condiciones anóxicas. A pH ácido el ión ferroso sí es estable, y puede ser oxidado por las bacterias.
Pueden usar también el manganeso, y algunas oxidantes del azufre pueden crecer también oxidando el hierro. Un ejemplo es Acidithiobacillus ferrooxidans. Su cadena de transporte de electrones es muy corta, con citocromos C y A1 y una proteína periplasmática llamada rusticianina, que contiene cobre. Los electrones pasan desde la rusticianina al citocromo C y de éste al citocromo oxidasa terminal (A1), tomando protones del citoplasma para formar el agua. Se sintetiza poco ATP.
El potencial del par Fe2+/ Fe3+ es muy alto, por lo que la cadena es más corta al estar más próximo al par O2/ H2O. No pueden reducir por tanto al NAD+, por lo que necesitan transporte inverso de electrones con consumo de ATP. Estudios bioquímicos sugieren que para formar ATP deben usar también el gradiente de protones preexistente en la célula, ya que hay una gran diferencia de pH entre el interior (6) y el exterior (2).
Oxidación de compuestos reducidos de nitrógeno
Los compuestos nitrogenados más comunes que se utilizan como donadores de electrones son el amoníaco y el nitrito, oxidados por bacterias quimiolitotróficas de dos tipos: nitrosoficantes y nitrificantes: Nistrosomonas y Nitrobacter, respectivamente. La oxidación de nitrógeno no se da en la naturaleza en un solo paso, sino que se realiza por la acción secuencial de estos dos grupos de microorganismos.
Bacterias nitrosoficantes
La oxidación del amoníaco requiere oxígeno molecular en una primera etapa catalizada por la amoníaco monooxigenasa (integral en la membrana). Esta enzima requiere NADH. El producto obtenido es la hidroxilamina; no se genera energía en esta fase. Esta molécula se oxida posteriormente hasta nitrito por la hidroxilamina-óxidorreductasa, periplasmática.
Derivados de esta oxidación se liberan 4 electrones que son cedidos a un citocromo C periplasmático: dos siguen la ruta hasta el oxígeno (pasan a otro citocromo C en la membrana y de éste al citocromo oxidasa terminal A1) y los otros se desvían para la reducción del oxígeno hasta agua a través de una ubiquinona (vuelven a la amoníaco monooxigenasa). El transporte de electrones permite la síntesis de ATP, y el poder reductor es generado por transporte inverso de electrones. El par redox NO2-/NH3 tiene un potencial demasiado alto para permitir la reducción directa del NAD+ a NADH.
Bacterias nitrificantes
La oxidación del nitrito se lleva a cabo en una sola etapa por la nitrito óxidorreductasa (NOR). Los electrones se transportan hasta el oxígeno por una cadena muy corta. Se genera poco ATP por fosforilación oxidativa. Se obtiene menos energía que en el caso anterior. El poder reductor se obtiene por transporte inverso de energía. Obtienen tan poco ATP que se ve reflejado en su bajo rendimiento de crecimiento. Quizá por esto algunas como Nitrobacter pueden crecer de forma quimioheterótrofa.
Ambos tipos de bacterias son aerobias estrictas y la mayoría autótrofas obligadas. Otras son mixótrofas. El proceso global es la nitrificación.
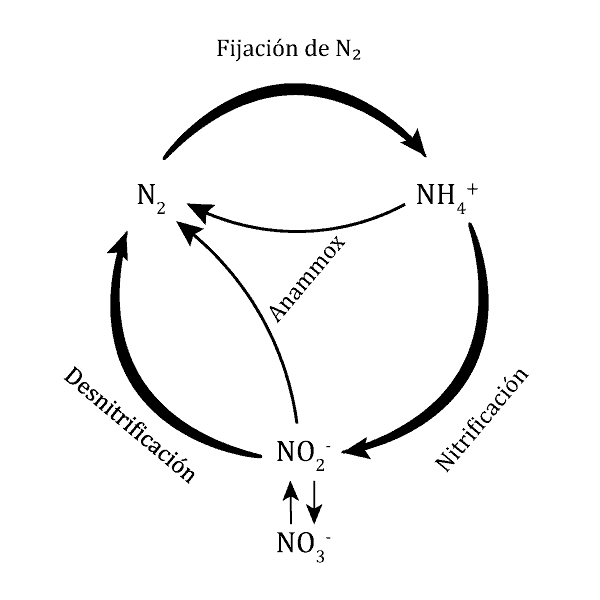
Anammox
Es la oxidación anóxica de amoníaco o ion amonio (NH4+). Es un proceso altamente exergónico. La reacción, con un ∆G0' de -357 kJ, es la siguiente:
NH4+ + NO2- → N2 + 2 H2O
Los organismos que la llevan a cabo, como Brocadia anamoxidans son particulares. Brocadia no tiene nada que ver con las bacterias oxidadoras aerobias del nitrógeno. Son miembros filogenéticamente muy relacionados con Planctomyces (mismo phyllum, dentro del volumen V del Manual de Bergey).
Contienen compartimentos rodeados de membrana, con una estructura análoga al núcleo de la célula eucariota. Poseen un compartimento denominado anamoxosoma, donde se localiza la reacción anamox. El nitrito de esta reacción procede de la oxidación del amoniaco llevada a cabo por las bacterias nitrosoficantes. Ambos organismos viven juntos en aguas con abunante amoniaco. Pueden encontrarse en suspensión partículas con zonas aerobias y zonas anaerobias. Brocadia también es autótrofa.