Tras ver la teoría sobre colorantes y tinciones vamos a analizar las principales tinciones usadas en microbiología y los colorantes que las forman.
En este caso, las diferentes técnicas de tinción analizadas se usan para el microscopio óptico. La mayoría de las muestras se podrán ver en el microscopio con aumentos de 20x y 50x, aunque habrán casos donde será necesario usar el aumento 100x (donde se añade también el aceite de inmersión a la muestra).
Las tinciones principales son la de Gram y de Ziehl-Neelsen, ambas diferenciales; aunque también hay otras tinciones diferenciales y selectivas de interés para la microbiología.
Recordatorio: antes de leer este artículo sería bueno que conozcas un poco de teoría sobre las fases, mecanismos y tipos de tinciones que hay (además de las partes que tienen los colorantes). Si conoces todo esto podrás entender mejor ciertas expresiones que son más del gremio 😄.
Índice de contenidos
Tinción de Gram
La tinción de Gram es probablemente la más conocida; es de tipo diferencial y sirve para distinguir a los microorganismos por morfología y composición.
Hay que tener en cuenta que se debe hacer la tinción cuando el cultivo esta en fase exponencial, ya que en fase estacionaria (“vejez”) se pueden confundir las gram positivas con las negativas. Esto ocurre debido a la perdida de capas de peptidoglicano por parte de bacterias gram positivas.
Colorantes
- Cristal violeta. Da color azul o violáceo a las bacterias gram positivas.
- Safranina. Da color rojizo o anaranajado a las bacterias gram negativas.
Aparte de estos colorantes, en la tinción de Gram se usará el lugol como mordiente, y alcohol 96% para decolorar. Todas las células (sean Gram positivas o negativas) se teñirán con el cristal violeta.

Ahora bien, el alcohol quita fosfolípidos y cierra los poros de la pared celular, por lo que el cristal violeta queda atrapado. Las bacterias gram positivas podrán soportar este proceso gracias a su gran capa de peptidoglicano. No obstante, las bacterias Gram negativas no aguantarán este tratamiento con alcohol, por lo que se quitará el cristal violeta de ellas.
Preparación
El proceso de tinción consta de los siguientes pasos:
- Con el asa de cultivo se cogen varias cargas (colonias, células bacterianas), y se extienden por el portaobjetos. No se añade agua destilada.
- El proceso de fijación se realiza por calor a la llama.
- Se añade cristal violeta, recubriendo con este colorante el portaobjetos durante 2 o 3 minutos.
- Ahora se añade lugol (yoduro potásico 2% + yodo) durante 1 minuto. El lugol no es un colorante en sí, sino que hace de mordiente. El mordiente se acopla con el colorante y facilita su absorción por parte del microorganismo.
- Se lava el portaobjetos con agua destilada. El agua no debe tocar directamente la muestra.
- Decolorado con alcohol 96%. Se añade el alcohol gota a gota, y de la muestra saldrán gotas violáceas. Paramos de añadir alcohol cuando salga la primera gota transparente de la muestra.
- Se añade el colorante de contraste, la safranina, durante 5 minutos.
- Por último se lava el portaobjetos y se seca.
Utilidades
La principal utilidad de la tinción de Gram es la de distinguir entre bacterias gram positivas y negativas. Las gram negativas que perdieron coloración por el tratamiento con alcohol ahora se verán de color rojo, naranja o rosáceo por acción de la safranina. Por otra parte, las bacterias gram positivas teñidas con cristal violeta tendrán un color azulado o violáceo.
Gram positivas
Las siguientes especies son las gram positivas más representativas:
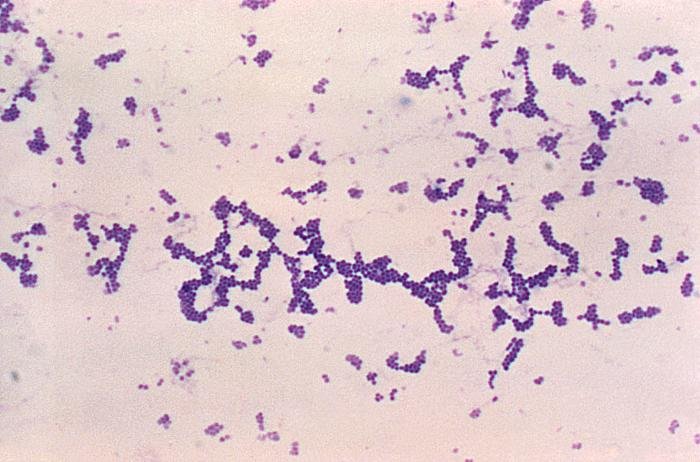
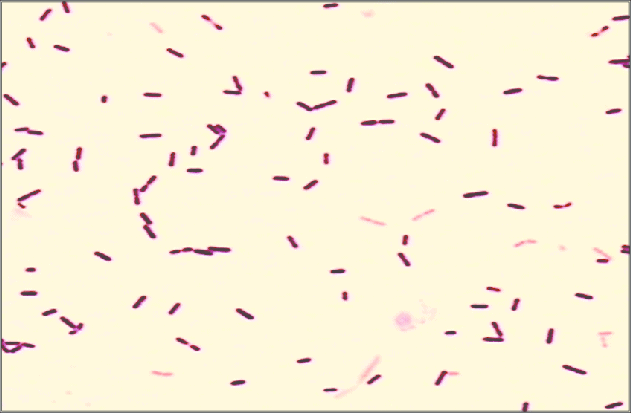
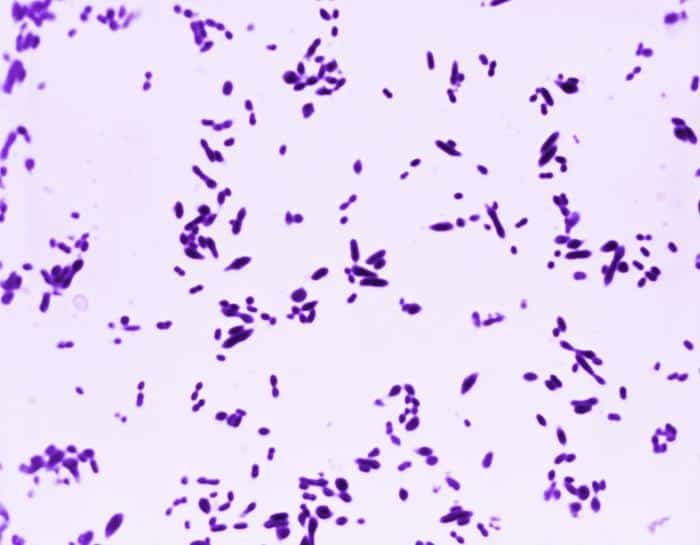
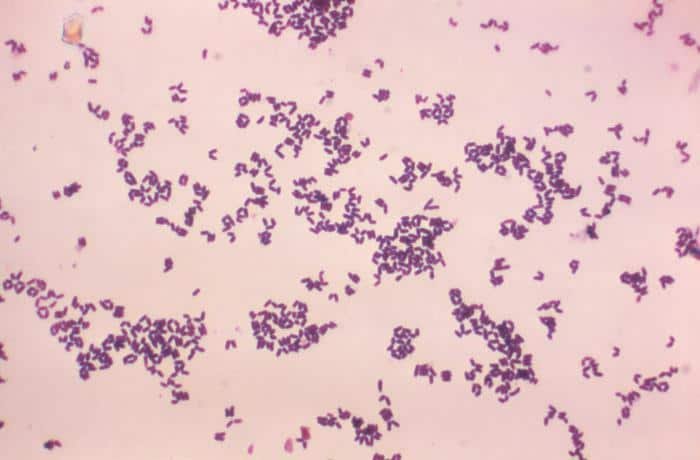

Quizá eches de menos a Mycobacterium tuberculosis. Es cierto, que es una bacteria gram positiva. No obstante, no se detecta bien con la tinción de gram. Hace falta otra tinción diferencial (tinción de Ziehl-Neelsen) que veremos más adelante.
Gram negativas
A continuación veremos algunas de las bacterias gram negativas más comunes:
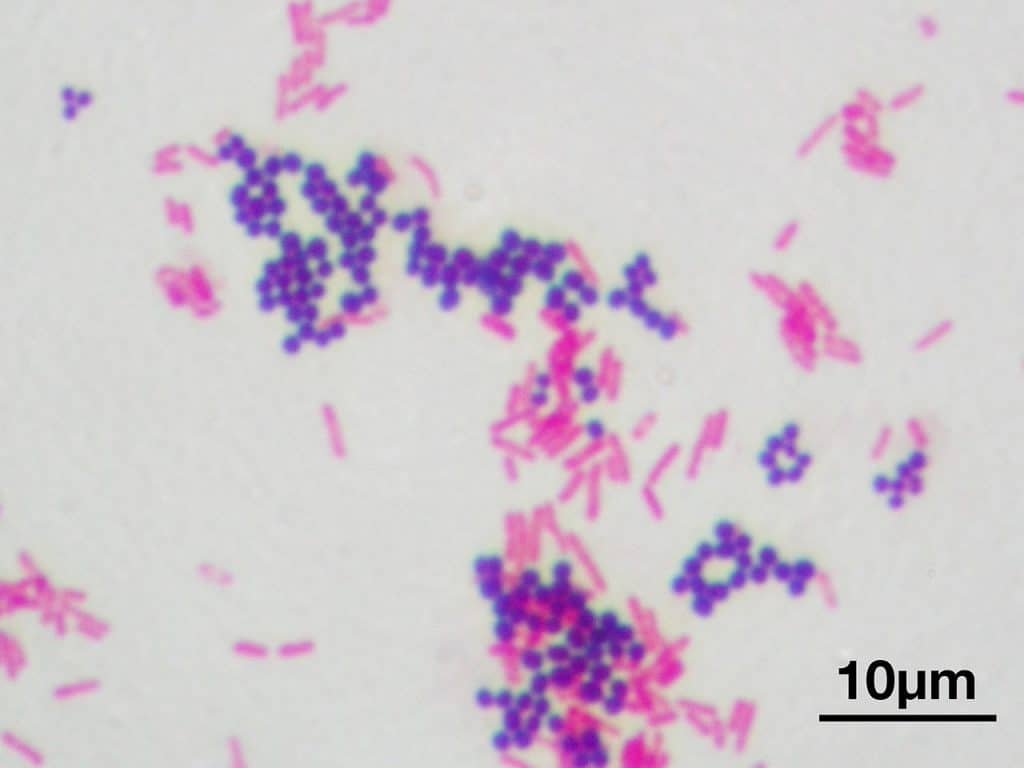
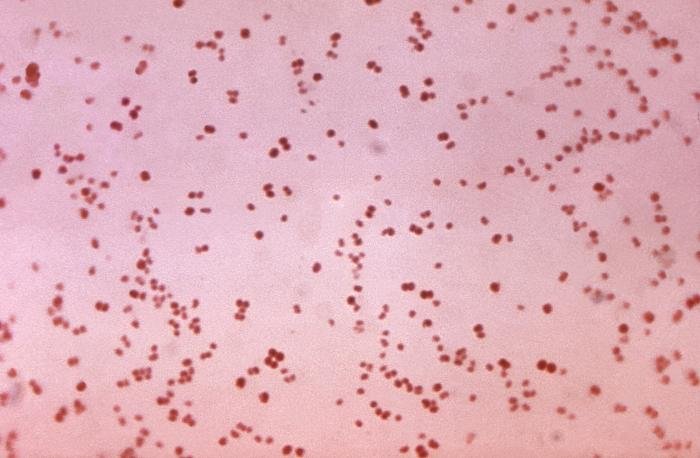
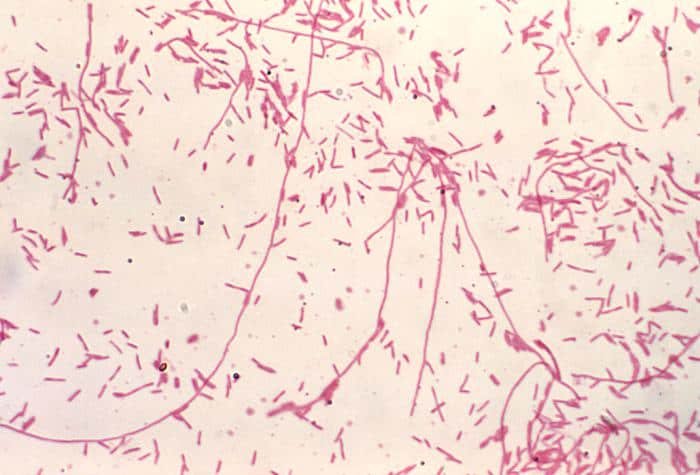

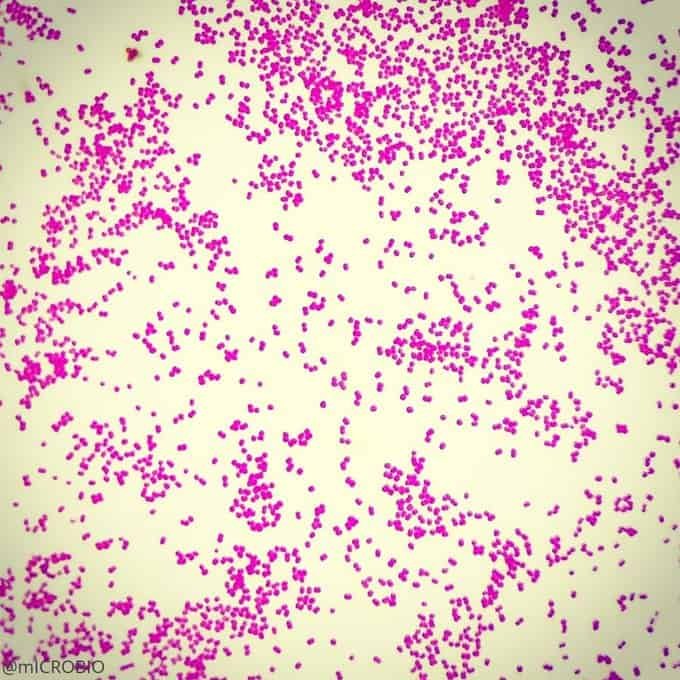
Recordatorio: las bacterias gram positivas se tiñen de azul (azul oscuro o violeta), mientras que las bacterias gram negativas se tiñen de rojo (rojo, anaranjado o rosado). A lo mejor lo tienes claro; pero en mi caso personal casi siempre las confundía. Por eso he puesto el color respectivo en cada frase, para que lo recuerdes mejor si te pasa igual que me pasaba a mí. 😉
Tinción Ziehl-Neelsen
La tinción de Ziehl-Neelsen es de tipo diferencial, y sirve para detectar bacterias ácido-alcohol resistentes (BAAR), siendo la más destacada Mycobacterium tuberculosis. Esto es muy útil, sobre todo teniendo en cuenta que M. tuberculosis no puede ser detectada correctamente con la tinción de Gram.
Lo que hace diferentes a estas bacterias es la presencia de un polímero (ácidos micólicos) que se une a azúcares, lo que provoca que el conjunto de la pared sea muy impermeable.
Colorantes
- Fucsina fenicada. Da un color rojizo a las bacterias AAR.
- Azul de metileno. Da un color azulado al resto de bacterias que no son AAR.
En la tinción de Ziehl-Neelsen, el alcohol-ácido cumple la una función parecida a la del alcohol 96% en la tinción de Gram. En este caso, el contraste aparece por los ácidos micólicos, que hacen que sus bacterias sean impermeables al alcohol-ácido. Las bacterias que no cuenten con estos ácidos micólicos se decolorarán por acción del alcohol, y la fucsina saldrá de éstos.
Preparación
El proceso de tinción consta de los siguientes pasos:
- Con el asa de cultivo se cogen varias cargas (colonias, células bacterianas), y se extienden por el portaobjetos. No se añade agua destilada.
- Se fija la muestra con calor.
- Se añade fucsina fenicada, cubriendo totalmente el portaobjetos durante 3 minutos.
- Más tarde, se pasa el mechero varias veces, durante 5 minutos, pero sin permitir que hierva el colorante, ni que se seque, ya que sino el colorante se consume.
- El exceso de colorante se quita con agua destilada.
- Se añade alcohol-ácido para la decoloración durante 10 minutos a intervalos de 1 minuto y medio.
- Ahora se añade el colorante de contraste, el azul de metileno, durante 3 minutos.
- Por último, se lava el portaobjetos y se seca al aire.
Utilidades
La principal función de la tinción de Ziehl-Neelsen es la detección de micobacterias, tales como las provocadoras de tuberculosis (M. tuberculosis) o la lepra (M. leprae). También hay otras micobacterias que, si bien no son patógenas, sí que pueden ser patógenos oportunistas en determinadas circunstancias.
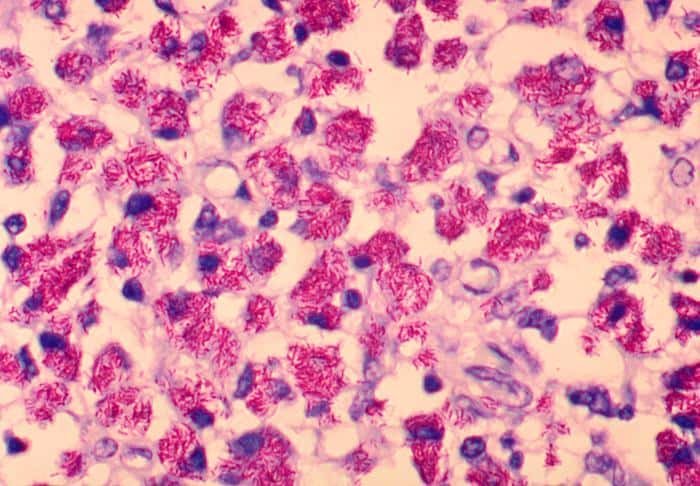
Además, se pueden detectar corinebacterias de gran interés para la biotecnología por su producción de aditivos, o a Streptomyces, formadora de diversos antibióticos. Nocardia y Actinomices también pueden aparecen como bacterias ácido-alcohol resistentes.
Las células bacterianas teñidas con fucsina aparecerán con un color rojo fuego, mientras que las teñidas con azul de metileno tendrán un color azulado.
Tinción de Wirtz-Conklin
La tinción de Wirtz-Conklin se usa para observar bien las endosporas bacterianas. La muestra debe ser obtenida de un cultivo en fase estacionaria. En este caso, para su observación al microscopio hay que usar la lente x100, usando aceite de inmersión.
Entra en el grupo de las tinciones selectivas, aunque al añadir un colorante de contraste es tecnicamente una tinción diferencial.
Colorantes
- Verde malaquita. Tiñe las endosporas de verde.
- Safranina. Es opcional, y sirve para colorear el resto de la célula con un color anaranjado.
Preparación
El proceso de tinción consta de los siguientes pasos:
- Con el asa de cultivo se cogen varias cargas (colonias, células bacterianas), y se extienden por el portaobjetos. No se añade agua destilada.
- Se fija la muestra con calor.
- Se añade verde malaquita, cubriendo totalmente el portaobjetos durante 9 minutos.
- Ahora se aplica calor de 3 a 6 minutos para que el colorante entre en las paredes de la endospora. El calor es aplicado hasta que aparezcan emisión de vapores.
- Se lava con agua el portaobjetos para retirar el colorante de la célula (a excepción de las endosporas).
- Ahora se añade el colorante de contraste, la safranina, durante 5 minutos.
- Por último, se lava con agua y se seca el portaobjetos.
Utilidades
Se usa para observan las endosporas bacterianas, estructuras de resistencia que forman algunas bacterias para sobrevivir en condicione ambientales extremas donde no pueden hacer su ciclo de vida normal. Así, se pueden ver las endosporas que forman Bacillus anthracis y Clostridium perfringens, entre otros.
Las endosporas no absorben la mayoría de los colorantes debido a sus cubiertas gruesas e impermeables. No obstante, el verde malaquita puede hacerlo, por lo que las endosporas bacterianas quedarán teñidas de verde mientras que el resto de las células bacterianas tendrán un color rosáceo.

Tinción de Leifson
La tinción de Leifson usa para la observación de flagelos bacterianos; entra dentro de las tinciones selectivas. Tienen un espesor de 0.01 micrones, por lo que son invisibles al microscopio óptico; por ello hace falta esta técnica especial. Para su observación en el microscopio óptico, se debe usar aceite de inmersión y el aumento 100x.
Recalcamos el hecho de esta tinción se usa para ver flagelos bacterianos; los flagelos de organismos eucariotas son más gruesos y pueden verse con tinciones simples o incluso con preparaciones al fresco.
Colorantes
Se usa el colorante de Leifson que está formado por:
- Fucsina básica 95%. Es el colorante en sí mismo.
- Etanol 1.2%.
- Ácido tánico 3%. Tiene función de mordiente.
- Cloruro sódico 1.5%.
- Agua destilada. Aparece en unión a ácido tánico y cloruro sódico, formando parte de sus soluciones.
Las estructuras teñidas aparecen con color rojizo.
Preparación
El proceso de tinción consta de los siguientes pasos:
- Con el asa de cultivo se cogen varias cargas (colonias, células bacterianas), y se extienden por el portaobjetos. No se añade agua destilada. (Previamente se debe haber hecho un círculo en el portaobjetos).
- El proceso de fijación se realiza sin llama durante 5 minutos. No se usa el mechero ya que demasiado calor puede destruir los flagelos.
- Se añaden unas gotas del colorante de Leifson y se espera 15 minutos.
- Ahora se lava el portaobjetos con agua destilada y se seca
Utilidades
Esta tinción se usa para ver a los flagelos, algo esencial para identificar muchas especies. Y es que los flagelos pueden aparecen en número y disposición diferente en las bacterias, de ahí que sean una forma de clasificación de estas (para ver los tipos de bacterias según el número y disposición de flagelos puedes entrar en el artículo de la célula procariota, en la sección “flagelo”).
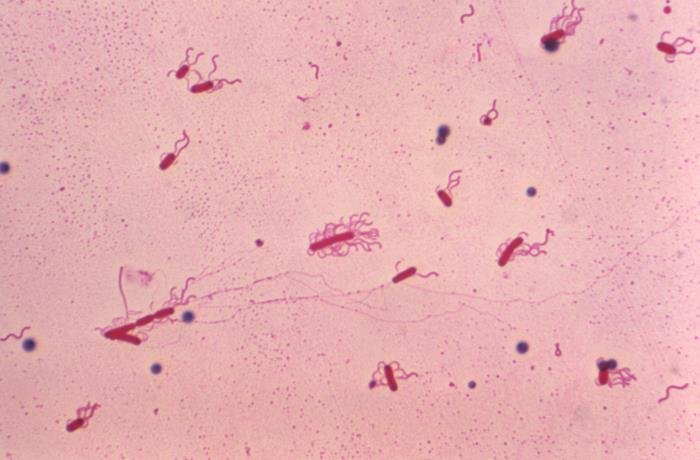
Tinción de Giemsa
Esta tinción es más usada en citología, ya que puede discriminar entre zonas con altos contenidos de ADN, por lo que puede diferenciar diversos orgánulos de la célula; es una tinción diferencial. No obstante, también se usa en microbiología para la detección de ciertas bacterias, destacando Rickettsia.
Colorantes
Colorante de Giemsa. Da un color azul oscuro o violáceo al microorganismo objetivo.
Preparación
El proceso de tinción consta de los siguientes pasos:
- Con el asa de cultivo se cogen varias cargas (colonias, células bacterianas), y se extienden por el portaobjetos.
- El proceso de fijación se realiza con metanol durante 3 o 5 minutos.
- Se añaden unas el colorante de Giemsa y se espera 8 minutos.
- Ahora se lava el portaobjetos con agua destilada y se seca
Utilidades
En microbiología, la tinción de Giemsa detecta a bacterias como Rickettsia y Chlamydia, a protistas como Plasmodium y Pneumocystis, y ciertos hongos, como Histoplasma. Dichos microorganismos se detectan en posibles células infectadas.

Otro patógeno importante que detecta la tinción de Giemsa es Helicobacter pylori, causante de gastritis y úlceras.

No obstante, esta tinción es más usada en citología.
Tinción negativa
Se usa para detectar las cápsulas que aparecen en algunas bacterias, así que entra en el grupo de las tinciones selectivas. La tinción negativa se puede usar para el microscopio óptico o para el microscopio electrónico.
Esta técnica se basa en contrastar las muestras mediante una sustancia opaca en ambos microscopios. Ahora bien, para el microscopio óptico se contrasta la muestra a los fotones, mientras que en el microscopio electrónico se constrasta la muestra a los electrones.
Colorantes
Para el microscopio óptico, principalmente pueden ser dos:
- Tinta china.
- Nigrosina.
Tiñen el fondo de negro.
Preparación
El proceso de tinción consta de los siguientes pasos:
- Se hace una preparación en fresco de la muestra.
- Ahora se añade tinta china.
- Ya se puede observar
Si, de todas las tinciones, es el proceso más corto que hemos visto.
Utilidades
La principal función de la tinción negativa es observar las cápsulas bacterianas. Esto ocurre porque las cápsulas no absorben la tinta china, por lo que estas estructuras aparecen como zonas claras en un fondo negro, oscuro.
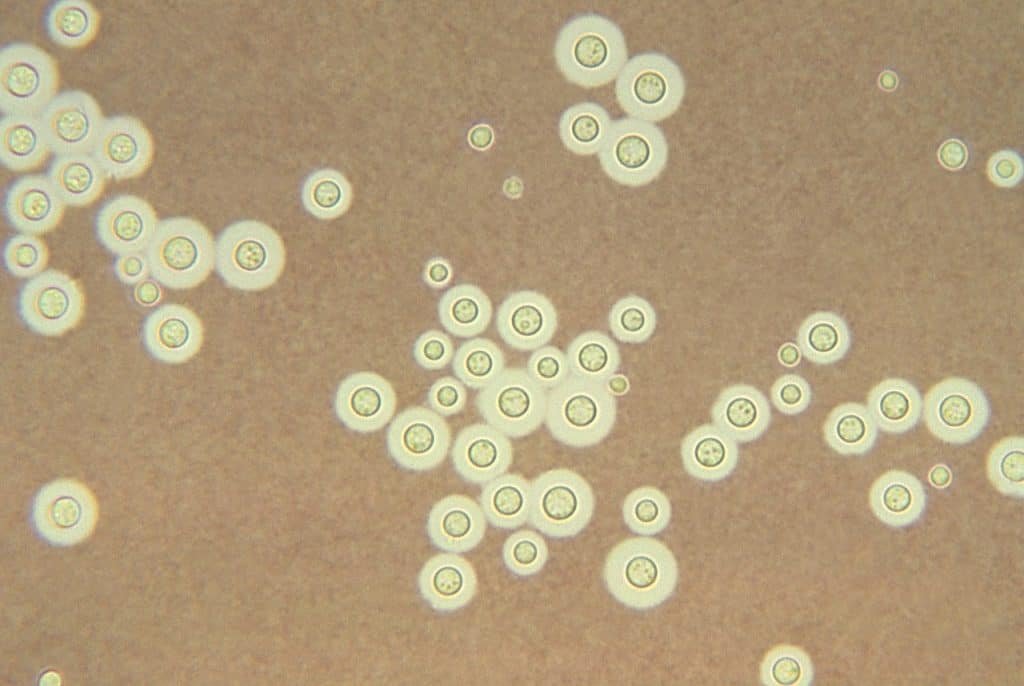
Ahora bien, se pueden añadir algún colorante de contraste para que las células bacterianas sean más visibles. Y, como ya hemos dicho, se puede usar nigrosina en vez de tinta china.
La observación microscópica es crucial en microbiología, permitiendo el estudio detallado de microorganismos. La evolución de los microscopios ha transformado esta disciplina, facilitando la identificación y caracterización de diversas especies.
Además, el uso de diferentes técnicas de tinción ha ampliado las posibilidades de análisis, permitiendo resaltar características morfológicas y estructurales que serían difíciles de apreciar sin estos métodos.
Índice de contenidos
Técnicas de observación microscópica
La microbiología esta indudablemente unida al progreso de los microscopios. De hecho, la historia de la microbiología como ciencia comienza con la creación de microscopios. Para observar mejor a los microorganismos se han desarrollado colorantes, tinciones diferentes que se usarán en función de nuestro objetivo.
Microscopios
Un microscopio es un conjunto de lentes que concentran y enfocan la luz sobre una muestra para formar imágenes visuales. El concepto de microscopio se basa en una propiedad física de la luz: la difracción. Cuando un rayo de luz pasa por dos superficies distintas, que produce una desviación que produce un retraso en la velocidad conocido como índice de refracción, producido entre dos medios cuando la luz pasa a través de ellos.
Fundamentos de microscopía óptica
- Ampliación o aumento. Número de veces que aparece resaltado el tamaño de un objeto y que es el producto de la lente ocular por la objetiva.
- Contraste. Diferencia de intensidad lumínica que hay entre la muestra y el medio. Para aumentar el contraste se recurre a medios de tinción.
- Poder de resolución (PR). Depende de:
- La longitud de onda (λ) de la luz visible usada (entre 0.4 y 0.7 µm)
- La apertura númerica (AN). Es igual a n*sen θ donde
- n. Es el índice de refracción del medio que atraviesa el haz, entre el cubreobjetos y el objetivo. Su valor es:
- 1. En el aire.
- 1.33. En agua.
- 1.5. En aceite de inmersión.
- θ. Es la mitad del ángulo del cono de luz que entra al objetivo desde la muestra.
- n. Es el índice de refracción del medio que atraviesa el haz, entre el cubreobjetos y el objetivo. Su valor es:
- Límite de resolución (LR). Es la distancia mínima que debe existir entre dos puntos para poder diferenciarlos como tales. La ecuación sería esta:
LR = λ / (2n * sen θ)
Con los microscopios normales no se puede observar a menos de 100nm; el objetivo máximo en un microscopio óptico es 100x (solo usando el aceite de inmersión, sino 50x).
Tipos de microscopios
- Microscopio de campo claro. Las muestras se visualizan al destacar sobre un fondo iluminado. Se puede aumentar el contraste sin necesidad de teñir. El contraste entre muestra y medio es muy pobre.

- Microscopio de fondo oscuro. Normalmente en las muestras el contraste entre la célula viva y el agua es muy difícil de resolver con un microscopio de campo claro. Pero este microscopio cambia las condiciones. Se coloca un condensador especial que impide el acceso de luz a la muestra directamente y sólo los rayos oblicuos que inciden son reflejados. Se enfoca un cono hueco de luz sobre la muestra, de modo que sólo la luz reflejada o refractada por la muestra puede formar una imagen. Se observa una imagen con un fondo oscuro y los rayos oblicuos hacen que la muestra se vea iluminada o brillante. Se usa para visualizar microorganismos que son difíciles de teñir por sus características o no se ven con el microscopio normal. Organismos frágiles o que se tiñen muy mal. Ejemplos: La bacteria de la sífilis (Treponema palium) o las espiroquetas que son muy delgadas.
- Microscopía de contraste de fases. Permite visualizar células sin necesidad de tinción. El condensador tiene un diafragma anular que produce un cono hueco de luz, y un objetivo con anillo de fase en una placa cambiadora de fase. Las células tienen un índice de refracción (n) distinto al del medio y desvían los rayos de luz que las atraviesan. La luz que pasa a través de una muestra sufre un retardo. A lo largo del microscopio se intercalan uno o más anillos de fase, que hacen pequeños retrasos en la refracción de la luz cuando pasa de un medio a otro, y los amplifica. Hay dos tipos de luz: la directa y la en fase (retardada). Cuando los dos tipos se integran en el ocular, forman una imagen muy contrastada con áreas muy iluminadas (en fase) y otras muy oscuras (fuera de fase), que va a permitir visualizar la morfología y tamaño de células y composición citoplasmática, Phb, gránulos de volutina, si hay endosporas en formación. Estos componentes no se observan de ninguna otra manera.
- Microscopio de interferencia diferencial. Este microscopio crea una imagen sobre la base de la detección de diferencias entre los n y el espesor de la muestra. Unos prismas generan dos ondas de luz polarizada plana en ángulo recto, una respecto de la otra. Una de las ondas pasa a través de la muestra, y la otra sirve de referencia, y pasa por una zona clara. Tras atravesar la muestra, las dos ondas se combinan e interfieren entre sí; llegan desfasadas al ojo y forman una imagen tridimensional. Si no hay muestra los dos haces llegan al mismo tiempo. Así, diversas estructuras aparecen claramente visibles, tales como paredes celulares, endosporas, gránulos, vacuolas y el núcleo de células eucariotas.
- Microscopio de luz UV. Utiliza una longitud de onda que está en el ultra violeta (200-300nm).
- Microscopio confocal. Usa como fuente de luz los rayos láser. Las muestras se marcan son fluorocromos en general. El rayo láser se dispone en todos los planos de la partícula, va analizando la muestra en distintos planos, y los superpone creándose un registro tridimiensional.
- Microscopía de fluorescencia. Consiste en detectar en la muestra qué emite luz, ya que ciertas moléculas y estructuras son fluorescentes y se excitan con energía radiante. Parte de esa energía que emiten es detectada por el microscopio (por ejemplo, la clorofila, que tienen sustancias fluorescentes naturales). En otras ocasiones se necesita marcar dichas estructuras o moléculas con fluorocromos, tales como la rodamina B o isotiocianato de fluoresceína para poder localizarlas. Un filtro excitador permite pasar la radiación excitada de la longitud de onda (λ) deseada, que es reflejada por el filtro dicroico, y enfocada por la lente del objetivo sobre la muestra. Las móleculas fluorescentes de la muestra se excitan y emiten luz de λ específica y mayor. Esta luz es enfocada por el objetivo y la mayor parte pasa a través del filtro dicroico y no se refleja. Un filtro de barrera final bloquea la luz residual con la frecuencia de la luz de exitación. Su aplicación es en especial en microbiología médica y ecología microbiana.
- Microscopio de fuerza atómica (AFM). Se fundamenta en las interacciones atómicas de las partículas de la muestra que son captadas por un dispositivo situtado muy cerca de la muestra. Se trata de una sonda que se va moviendo sobre la muestra y recoge datos de las repulsiones atómicas (ondas desprendidas). Todo lo que detecta el dispositivo se transmite a través de un sistema informático, y en una pantalla se muestran los resultados tridimensionales.
- Microscopía electrónica. Usa una corriente de electrones que se desplaazan a través de unos lentes electromagnéticos y se van a proyectar sobre una muestra extremadamente fina que tiene que estar en condiciones de vacio extremo.
- Microscopio electrónico de transmisión (MET). Se puede aumentar el contraste mediante la tinción negativa, o los métodos de sombrado o criofractura.
- Microscopio electrónico de barrida (MEB). Útil para ver estructuras en 3 dimensiones.
Microscopio óptico vs Microscopio electrónico
En la siguiente tabla se pueden ver las diferencias entre el microscopio óptico y el microscopio electrónico.
| MO | ME | |
| Aumento | 1.000-1.500 | > 100.000 |
| Resolución máxima | 0,2 µm | 0,5 nm |
| Fuente de radiación | Luz visible | Haces de electrones |
| Lentes | Lentes de vidrio | Lentes electromagnéticas colocadas simétricamente respecto al eje axial que enfocan el haz de electrones, a través de un tubo en el que se ha hecho vacío, sobre la muestra. |
| Fuente de contraste | Absorción de luz diferencial | Dispersión de electrones |
| Medio de desplazamiento | Aire | Alto vacío |
| Montaje de la muestra | Portaobjetos | Rejillas metálicas Tratamiento previo de las muestras |
Observación de microorganismos. Preparaciones
Basicamente, se pueden observar a los microbios mediante 2 tipos de preparaciones:
- Preparación húmeda o fresca. En esta se observan los microorganismos vivos. Es típica de los microscopios de campo oscuro y de contraste de fases. Se usa en caso de que la morfología se altere al usar alguna tinción. Sirve para determinar la movilidad u observar cambios citológicos o algunas inclusiones.
- Preparación teñida. Permite ver a los microorganismos en función de su capacidad para retener o no determinados colorantes. La principal ventaja es que aumenta el contraste, acentuando las características morfológicas pero conservandolas. Los colorantes se usan para formar las tinciones.
Colorantes. Tinciones
Para mejorar el contraste entre los microorganismos y el medio lo que hlacemos es recurrir a las tinciones, tratando las muestras celulares mediante colorantes que son sustancias con una afinidad especial por determinados componentes o estructuras celulares. Como resultado de la tinción lo que vamos a observar son muuestras de microorganismos teñidas más contrastadas sobre un medio difuso (no teñido). En microbiología vamos a utilizar siempre preparaciones fijadas, es decir, muestras de células muertas, y para las tinciones se utilizan colorantes (no tintes).c
Todo colorante lleva dos partes:
- Grupo cromóforo. Parte de la molécula responsable del color, es el radical cromóforo. Se trata de moléculas alifáticas que suelen llevar un doble enlace conjugado (N=N) o un grupo sulfo (SO2).
- Grupo auxocromo. Región de la molécula que no tiñe pero que facilita la interacción del radical cromóforo con la molécula que va a teñir. Suelen ser radicales iónicos (OH–, COO–, NH2+) muy activos con capacidad para interactuar.
Los colorantes se van a clasificar en función del grupo auxocromo:
- Grupo auxocromo ácido o aniónico (-). El grupo auxocromo es un anión y va a interaccionar con componentes celulares básicos de la célula, como el citoplasma y estructuras con carga positiva. Ejemplos: eosina, rojo-congo, fucsina, nigrosina.
- Grupo auxocromo básico o catiónico (+). El grupo auxocromo es un catión y va a interaccionar con regiones o zonas ácidas de la célula que tengan carga negativa, como con los ácidos nucleicos. En general todas las bacterias tienen una carga externa negativa: estos colorantes van a interaccionar sobre todo con la pared bacteriana. Ejemplo: safranina, azul de metileno, cristal violeta.
- Grupo auxocromo sin carga, liposoluble. Combinación de un anión y un catión que normalmente en solución para teñir se van a disociar en los dos átomos. Ejemplo: eosina de metileno, negro-sudán.
Fases de la tinción
Comprende varias partes:
- Extensión. Se toma la muestra y se extiende a lo largo del porta.
- Secado breve.
- Fijación. Normalmente se fijan suavemente con una llama, y es una fijación en un doble sentido: una fijación física que consiste en que la capa que hemos puesto quede pegada al cristal y una fijación biológica, de tal manera que cuando se aplica calor se desnaturalizan las estructuras celulares, se coagulan las proteínas en su conformación nativa de manera que ahora puedan tomar el colorante. Solo en algunos casos se puede acudir a una fijación química.
- Aplicación del colorante. Es el proceso de tinción en si mismo.
- Lavado.
- Observación.
Mecanismos de tinción
Fundamentalmente hay dos:
- Tinción por intercambio iónico. Si tenemos una bacteria con carga negativa y le añadimos azul de metileno, el grupo auxocromo desplaza a los cationes adheridos a la pared bacteriana y los sustituyen, liberándose cloruro sódico.
- Tinción por solubilidad diferencial del colorante entre la muestra y el medio. Las células en un medio acuoso tienen estructuras hidrofóbicas en su interior. Si teñimos con negro-sudán (que es lipofílico) no se disuelve en el agua y se une a las regiones hidrofóbicas (o con un alto contenido en lípidos), y así tiñe.
Tipos de tinciones
- Simple. Aplica un único colorante que tiñe completamente las células. Normalmente es con azul de metileno. No es muy útil (se obtiene información sobre la forma y variedad, pero poco mas).
- Diferencial. Incorpora 2 colorantes de forma excluyente (cada bacteria se teñirá con uno de ellos, pero no con los dos). Tinción de GRAM (1884) y tinción de Ziehl-Neelsen (para las bacterias acido-acohol resistentes).
- Específica o selectiva. El colorante se adhiere y tiñe determinadas estructuras especificas de la célula por las que tiene afinidad. Endosporas, volutinas, flagelos. Leifson, con rosanilina (que tiene acido tánico), aumenta la visibilidad del flagelo, que se fija con formol. Como ejemplos tenemos la tinción negativa, la de flagelos, o endosporas.
En el artículo que enlazamos a continuación podrás ver las tinciones y colorantes principales usados en microbiología.
Tinción de Gram
Data del año 1884, por Hans Christian Gram. La preparación consta de varias partes:
- Se prepara el frotis, y se tiñe en primer lugar con cristal violeta (generalmente durante 1min, aunque el tiempo depende de la pureza del colorante). TODAS las células se tiñen de color azul violeta.
- Se añade lugol, que es una solución de Iodo y ioduro potásico que tiene función de mordiente es decir se une con el cristal violeta y forma un complejo insoluble que queda atrapado y absorbido dentro de las células.
- Esta es la etapa crítica: decolorar con alcohol de 96º. Todas las células toman el primer colorante pero cuando le añadimos el alcohol, las GRAM- pierden el colorante, mientras que las GRAM+ siguen coloreadas.
- Ahora añadimos el colorante de contraste, en este caso, la safranina, la cual tiene que tener un grupo cromóforo que no sea violeta, que suele ser rojo rosa. Ahora las GRAM+ se ven color violeta y las GRAM- de color rosa.
Es preferible utilizar cultivos jóvenes, para evitar alteraciones en la pared y por lo tanto, confusiones. Si se abusa del alcohol se puede extraer la tinción de las GRAM+ por lo que hay que tener cuidado.
Para ver la tinción de Gram con más detalle tienes el siguiente artículo donde se analiza la tinción de Gram además de otras tinciones y colorantes usados en microbiología.
